众所周知,肿瘤嗜酸。
它嗜酸到什么程度呢?
这么说吧,即使在氧气充足的情况下,肿瘤也会启动糖酵解,生产大量的乳酸,把自己弄成“酸性体质”。
很多人可能还不知道,我们剧烈运动之后身体产生的乳酸虽然让我们肌肉酸疼的乳酸,但肿瘤却把乳酸当做大宝贝。
我们之前就介绍过肿瘤中乳酸的很多功能。例如,乳酸可以将瘤内的巨噬细胞从抗癌型变成促癌型,还可以增强调节性T细胞的免疫抑制功能,甚至还能导致PD-1抑制剂治疗失败。
让我没想到的是,上面的研究成果竟然还不是瘤内乳酸的全部手段。
今天,由苏州大学生物医学研究院周芳芳领衔的研究团队,在顶级期刊《细胞》上发表了一项重磅研究成果[1]。
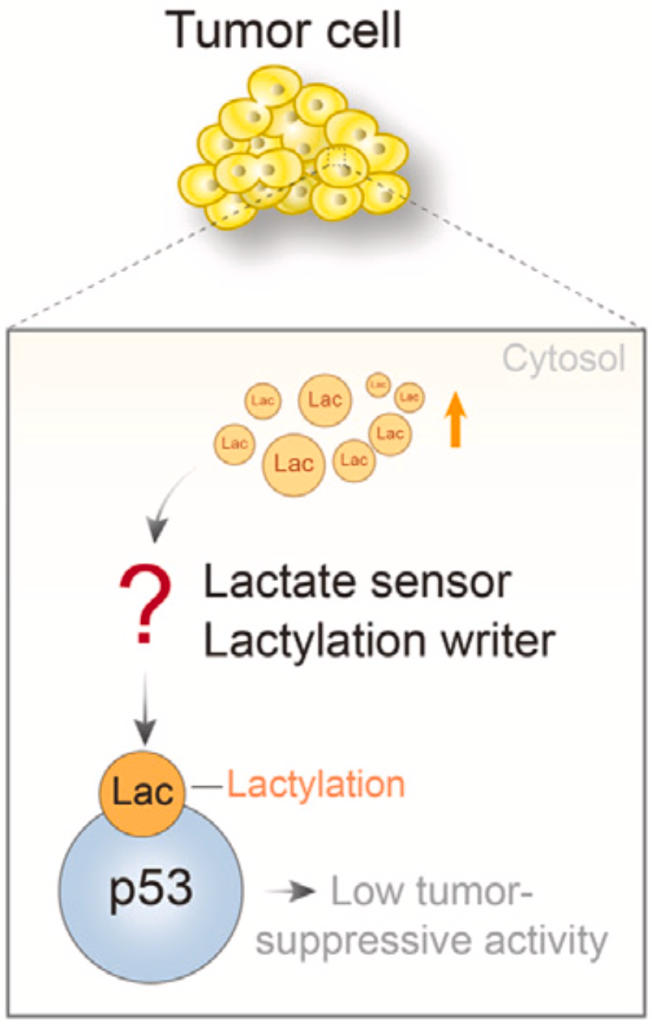
她们首次发现,肿瘤内的乳酸会被乳酸化酶AARS1识别,并添加到抑癌蛋白p53的DNA结合结构域的两个关键氨基酸上,导致抑癌蛋白p53因乳酸化而失活,最终促进癌症的进展。此外,她们还发现β-丙氨酸可以阻止AARS1对p53的乳酸化,为癌症的治疗提供了新思路。
苏州大学的Zong Zhi和谢枫是论文的共同第一作者。据了解,这也是苏州大学首次以第一单位在《细胞》上发表研究成果[2]。
正如文章开头说的那样,乳酸是促进肿瘤生长的重要代谢产物。
虽然背后的机制已经有很多研究,但是乳酸与抑癌蛋白p53之间是否有关系,如果有的话,又是如何发生关系的,以及对肿瘤的发生发展有啥影响,目前仍知之甚少。
周芳芳团队分析了癌症基因组图谱(TCGA)中的乳腺癌数据集,发现在p53正常的癌症患者中,血清乳酸水平高的患者,p53信号通路活跃程度较低。这似乎暗示,乳酸会抑制p53的功能。
基于肿瘤小鼠模型的实验发现,给小鼠注射乳酸钠之后,小鼠成瘤更快,肿瘤的体积也更大;更重要的是,p53蛋白的活性确实也被抑制了。值得注意的是,将生成乳酸的乳酸脱氢酶A(LDHA)敲除后,会导致肿瘤形成延迟、肿瘤乳酸和肿瘤负荷减少,以及p53活性增加。
以上研究结果说明,肿瘤产生的乳酸确实是抑癌蛋白p53的抑制剂。
那乳酸是如何影响p53蛋白活性的呢?
周芳芳团队先做了一个体外实验,发现用乳酸盐单独处理p53不会影响p53的活性;不过,一旦加入细胞裂解液之后,p53蛋白的活性就会受到乳酸盐的抑制,而且p53活性的降低,与p53的乳酸化水平增加有关。
基于细胞的实验也证实了上述发现。因此,研究人员认为,乳酸可在细胞中被感知,并通过乳酸化成为p53的一部分,进而使p53失活。
接下来就是要找到乳酸化p53的关键酶了。
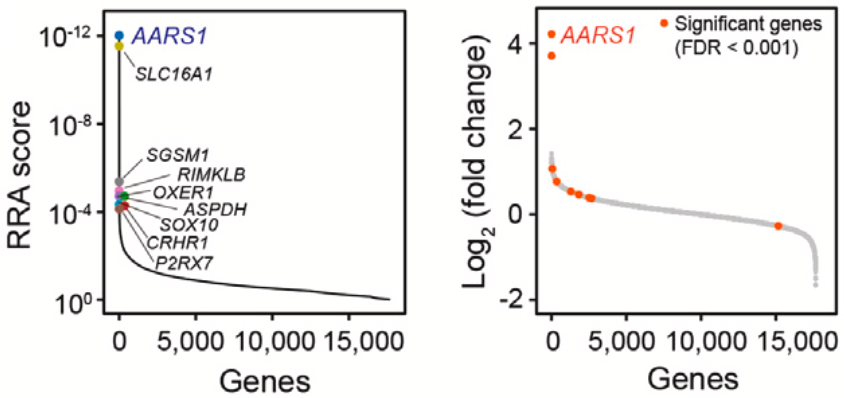
周芳芳团队用CRISPR基因编辑技术,在全基因组范围内展开了地毯式筛查,丙氨酰-tRNA合成酶1(AARS1)很快浮出水面。
在敲除AARS1后,肿瘤细胞在增殖、集落形成和异种移植肿瘤形成方面,均显著减弱。此外,AARS1缺失之后,乳酸钠促进肿瘤生长的能力也消失了。
以上研究结果说明,AARS1是乳酸依赖性p53失活和肿瘤生长所必需的。
随后,周芳芳团队揭示了AARS1乳酸化p53的机制。
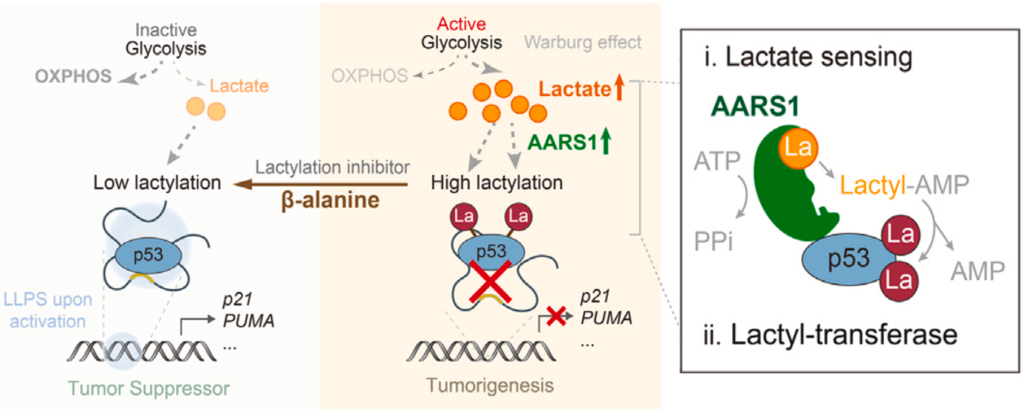
原来AARS1在识别到乳酸之后,会与乳酸结合,催化乳酸-AMP的形成,然后将乳酸转移到p53蛋白DNA结合结构域120(K120)和139(K139)号赖氨酸残基上,导致p53乳酸化,进而阻碍p53蛋白的液-液相分离(LLPS)、DNA结合和受调控基因的转录激活,最终达到抑制p53抑癌功能的效果。
好消息是,周芳芳团队发现AARS1的底物β-丙氨酸可以有效地抑制p53的乳酸化。
基于癌症患者的数据,研究人员还发现,在许多肿瘤类型中AARS1的表达水平都升高,并且与p53乳酸化水平升高、p53活性降低、以及野生型p53患者的生存率较差相关。
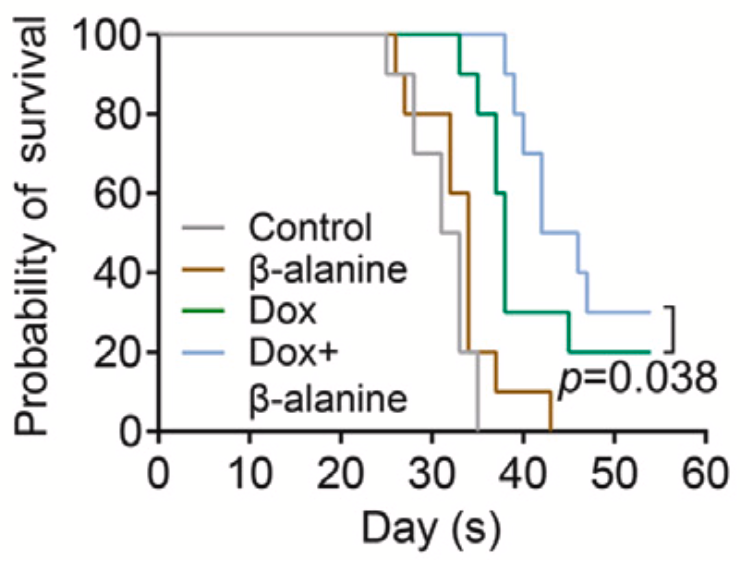
在研究的最后,周芳芳团队还测试了β-丙氨酸的抗癌潜力。她们发现,β-丙氨酸处理可适度抑制肿瘤细胞增殖、克隆形成和异种移植瘤的生长。值得注意的是,β-丙氨酸可以增强化疗药物多柔比星(DOX)在肿瘤小鼠模型上的抗癌效果。
总的来说,周芳芳团队的这项研究成果表明,肿瘤产生的乳酸会通过乳酸化作用拮抗p53的抑癌功能,并揭示了AARS1是p53乳酸化的关键酶,以及β-丙氨酸可以阻止p53的乳酸化。
这一机制的发现,让我们对肿瘤的糖酵解代谢有了新认知,也为癌症的治疗提供了新思路。
参考文献:
[1].Zong et al., Alanyl-tRNA synthetase, AARS1, is a lactate sensor and lactyltransferase that lactylates p53 and contributes to tumorigenesis, Cell. 2024. doi:10.1016/j.cell.2024.04.002
[2].https://ibms.suda.edu.cn/aa/81/c3463a567937/page.htm
文章来源:奇点网