阿尔茨海默病(AD)是一种非常典型的“老人病”,发病率会随着年龄的增长而迅速增加,但这是为什么却并不清楚。
今天,《自然》杂志发表了马克斯·普朗克研究所团队的新成果,科学家们发现,衰老会带来的髓鞘功能障碍可能是关键。研究发现,在AD模式小鼠中,髓鞘损伤会促进Aβ的产生和减少其清除,也就是说年龄相关的髓鞘缺陷会直接和间接地促进Aβ斑块的形成,是较为早期的AD风险因素。
论文题图
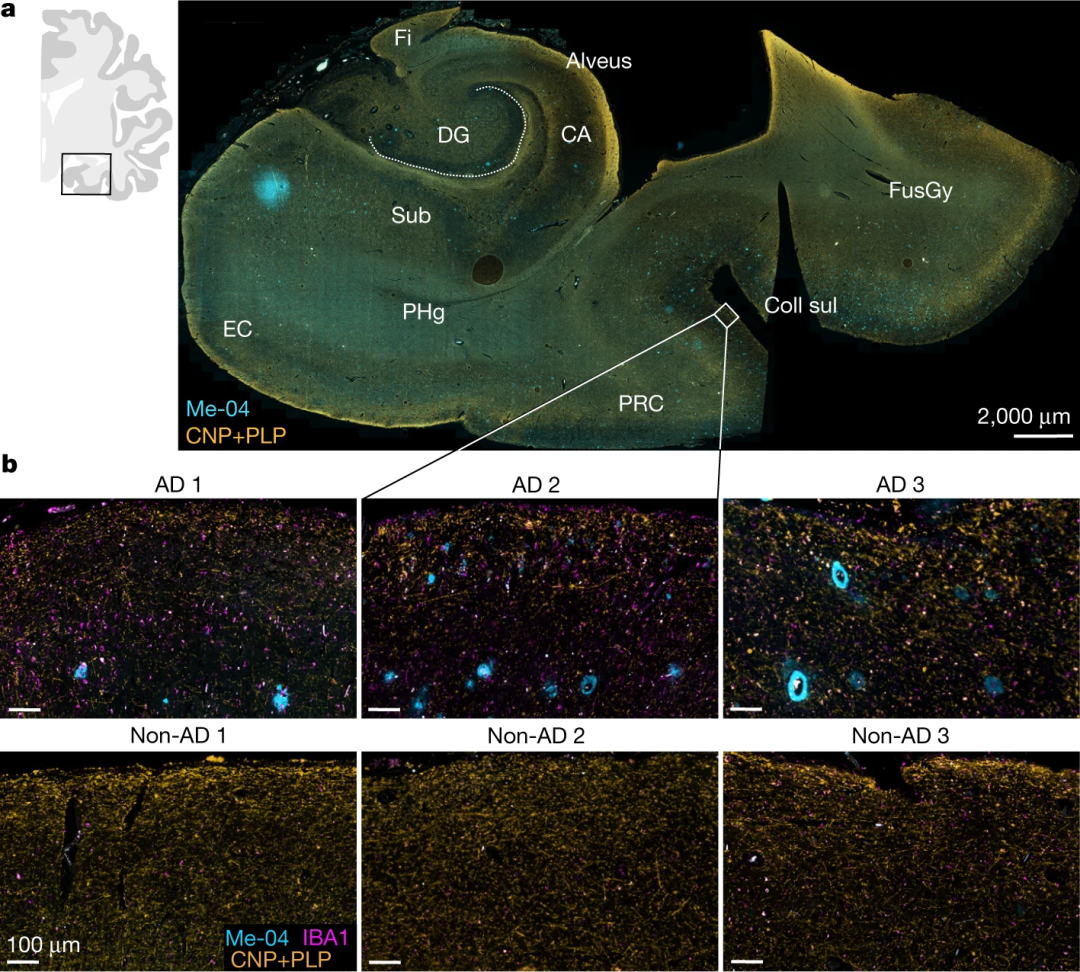
有一定的影像学研究证据表明,皮质髓鞘损伤发生在AD的临床前阶段。研究者们使用免疫荧光技术,详细分析了一组AD患者皮质样本,发现样本中髓鞘密度下降,而且不局限于斑块附近。此外,髓鞘丢失的部位也观察到小胶质细胞数量的增加。
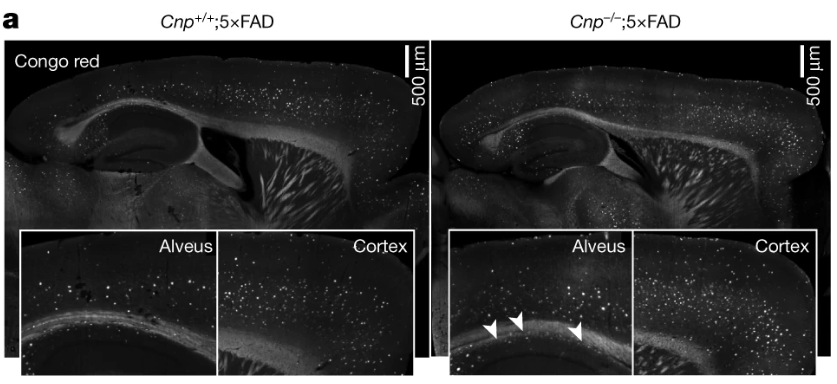
令5xFAD AD模式小鼠也具有同样髓鞘缺陷,研究者观察到它们在6月龄时海马白质和皮质中的淀粉样斑块负荷显著增加。这些小鼠在迷宫中也表现出了多动、缺乏焦虑感等典型的AD类行为缺陷症状。
研究者发现,在6月龄髓鞘缺陷AD模式小鼠中,β分泌酶和γ分泌酶聚集,可溶性APPβ片段显著增加,BACE1水平升高。且小鼠白质中APP代谢显著向羧基末端片段(CTF)丰度增加转移,全长APP丰度或α/β CTF比值不变。由此可见髓鞘功能障碍会影响到Aβ的生成。
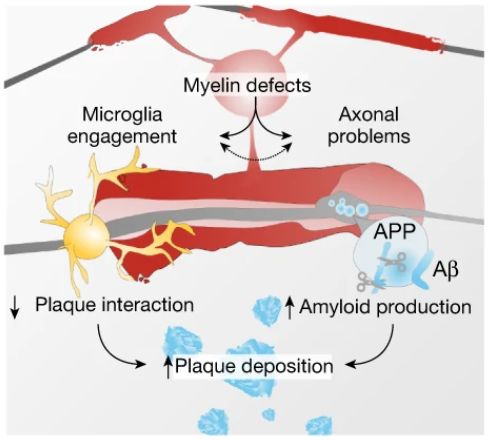
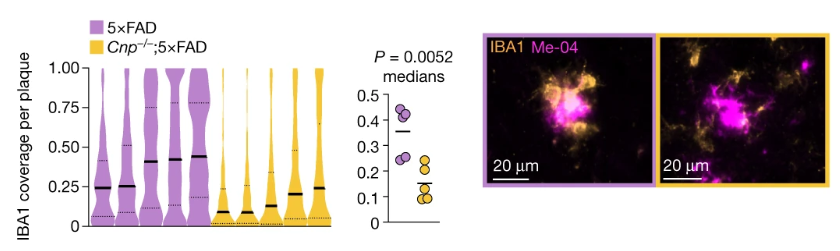
髓鞘缺陷也改变小胶质细胞的反应。小胶质细胞会在淀粉样蛋白斑块附近“合围”,清除垃圾碎片。但在髓鞘缺陷AD小鼠中,皮质中的小胶质细胞尽管数量有所增加,却无法聚集在淀粉样蛋白斑块周围。
小胶质细胞(土黄色)、淀粉样蛋白斑块(洋红色)
此外,有趣的是,研究者在一种无髓鞘的模式小鼠(EmxcreMbpfl/fl)中也进行了实验,却发现完全没有髓鞘反而延迟了5xFAD小鼠斑块的形成。不过研究者认为,这种无髓鞘小鼠最终形成的斑块形态和分布与正常的AD模式小鼠存在差异,表明二者之间斑块的形成机制并不一样。
研究者认为,以上研究结果说明,适量的、健康的髓鞘具有针对Aβ的保护作用,而年龄相关的髓鞘完整性丧失可能是淀粉样蛋白沉积的驱动因素。这也改变了既往认为少突胶质细胞在AD进展中作用不大的观点。如果后续能够在人类中也观察到髓鞘对AD进展的关键作用,那么我们就又多了一个可用的治疗靶点了。
参考资料:
[1]Depp, C., Sun, T., Sasmita, A.O. et al. Myelin dysfunction drives amyloid-β deposition in models of Alzheimer’s disease. Nature (2023). https://doi.org/10.1038/s41586-023-06120-6
文章来源:奇点网