非靶向代谢组学(Untargeted metabolomics)是一种分析生物样本中所有可检测代谢物的方法。其中LC-MS非靶向代谢组学是一种利用液相色谱-质谱联用技术(LC-MS)无偏向性地检测生物体内所有小分子代谢物的动态变化的技术。由于环境对生物体的影响会最终体现为代谢物的变化,因此LC-MS非靶向代谢组学在动物生长发育、疾病生物标志物(Biomarker)筛选、药物研发等领域的应用越来越广泛。
一、原理简介
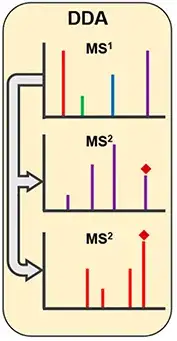
LC-MS非靶向代谢组学采用高效液相色谱作为分离系统,以高分辨率质谱为检测系统,对样本中的代谢物进行分析检测。质谱检测主要是基于被测代谢物的质荷比(m/z)不同,选择数据依赖性扫描方式(DDA)对代谢物进行扫描,即对选定范围内质荷比的母离子进行全扫描,获得一级谱图,然后从全扫描质谱中选择的多个母离子进行二级扫描,获得二级谱图。最后使用一级谱图和二级谱图与数据库匹配进行代谢物的鉴定和定量分析。该技术具有样品前处理简单、检测范围广、分离能力强等优点,是代谢组学研究中常用的分析手段。
二、技术路线
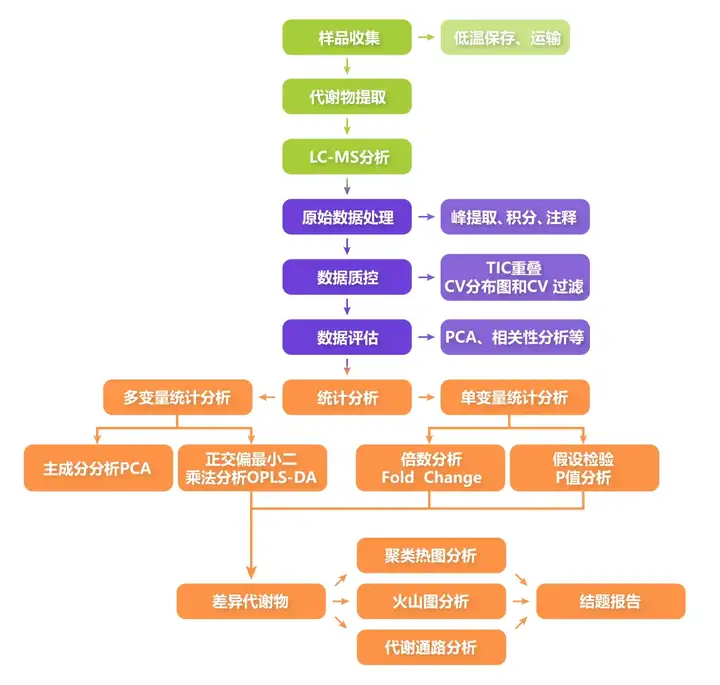
LC-MS非靶代谢组学的技术路线包括实验检测和数据分析两大部分,其中实验部分包括样本收集、代谢物提取、代谢物检测,数据分析包括原始数据的处理、数据质控、数据评估、统计分析。统计分析通过单变量统计分析和多变量统计分析方法,筛选出组间差异的代谢物,然后对其代谢通路进行分析。
三、检测物质类型
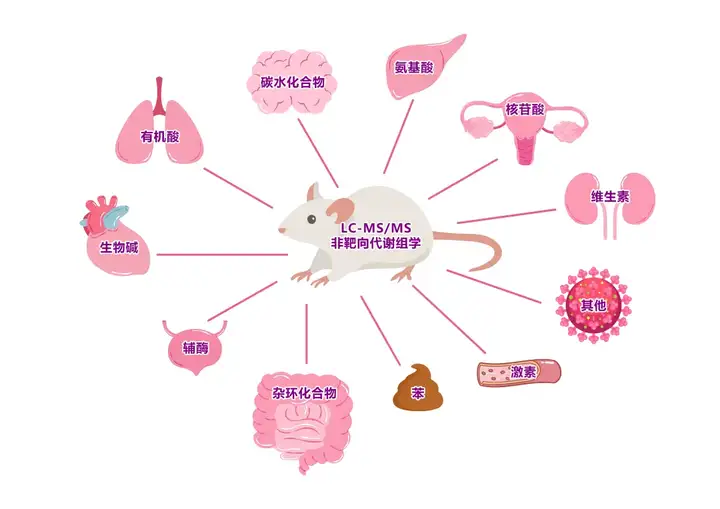
LC-MS非靶向代谢组学检测的物质类型包括碳水化合物及其代谢物、氨基酸及其衍生物、有机酸及其衍生物、核苷酸及其衍生物、生物碱类、辅酶和维生素类、激素及其相关物质、苯及其衍生物、杂环化合物等多种化合物。
四、揭秘项目实测数据
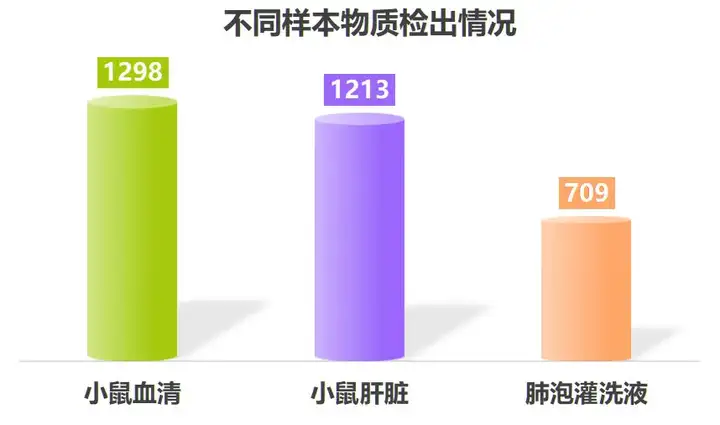
我司对小鼠血清、肝脏、肺泡灌洗液样本进行LC-MS非靶向代谢组学检测,发现小鼠血清检出1298种代谢物,小鼠肝脏检出1213种代谢物,肺泡灌洗液检出709种代谢物。样本代谢物的检出情况与样本的处理、组织类型等相关,因此上面数据仅供参考。
五、文献案例

2023年7月29日,上海交通大学医学院附属仁济医院李海教授团队在Journal of Hepatology(IF:26.8)上发表了题为“Metabolic biomarkers significantly enhance the prediction of HBV-related ACLF occurrence and outcomes”的研究性论文。
1、研究背景
慢加急性肝衰竭(acute-on-chronic liver failure, ACLF)是发生在慢性肝病患者中的一种短期死亡率高、以器官衰竭和高全身炎症反应为特征的临床综合征。提高ACLF生存率的最大潜力是通过早期诊断和准确预后,实现对疾病的最佳管理。传统的肝硬化评分系统,对ACLF预后的准确性有限。在中国和其他亚洲国家,慢性乙型肝炎是ACLF(HBV-ACLF)的主要病因,目前ACLF尚无有效的治疗方法。早期诊断和准确的预后对改善ACLF患者的临床预后至关重要。本研究旨在发现新的生物标志物来提高HBV-ACLF早期诊断和预后的准确性。
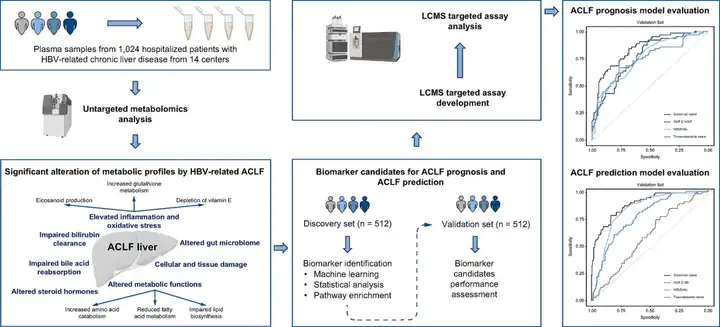
2、研究结果
(1)患者队列和研究设计
该研究共有源于大型多中心前瞻性研究(CATCH-LIFE队列)于入院时采集的1024份慢性乙肝急性加重的样本,包括367例ACLF患者(127例未存活,240例在入院90天内存活)和657例非ACLF患者(135例在住院期间发展为ACLF,522例病情稳定)。
总结HBV-ACLF和非ACLF患者入院时的关键临床参数,其中,HBV的免疫状态标记物(HBeAg和HBeAb)无显著性差异,HBV-ACLF患者器官衰竭比例显著增加,总胆红素(TB)、丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)、肌酸、国际标准化比率(INR)、C-反应蛋白(CRP)指标水平升高,终末期肝病肝硬化评分模型(MELD-Na)和欧洲慢性肝衰竭研究基金会-慢加急性肝衰竭(CLIF-C ACLF)评分较高。非幸存者的TB,INR,CRP,MELD-Na和CLIF-C ACLF的评分高于幸存者。ACLF前患者的TB,INR和MELD-Na的评分高于稳定的非ACLF前患者。
接着对1024份的血浆样本进行非靶向代谢组学分析。将样本随机分为相等的两半分别作为发现集和验证集,并通过机器学习等统计分析方法明确与ACLF组90天内死亡和非ACLF组28天内进展为ACLF相关的代谢物,且在验证集中评估(图6)。
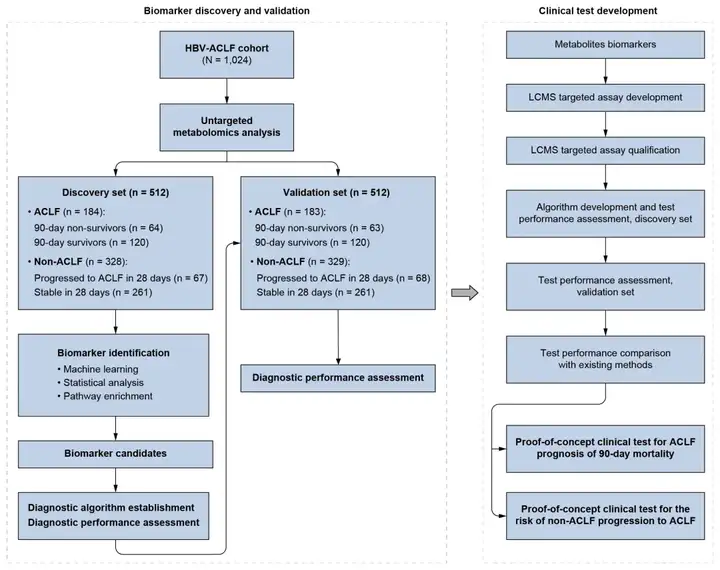
(2)HBV-ACLF显著改变了血浆代谢组
将发现集的512例样本进行非靶向代谢组学检测,共鉴定出1072种物质,其中有715种差异代谢物(图7 A),ACLF分别影响了脂质、氨基酸、外源性物质、核苷酸、辅助因子和维生素、碳水化合物、多肽、部分表征分子、能量代谢等途径(图7 B)。通过代谢通路研究发现在ACLF患者存在七方面的发病机制:组织与细胞的严重损伤;明显增加的高炎症反应和氧化应激;氨基酸分解、脂类合成以及脂肪酸代谢明显异常影响线粒体等细胞器的细胞能量;激素水平的明显紊乱;胆红素清除明显异常;胆汁酸重吸收明显紊乱;肠道微生物的明显异常(图7 C)。
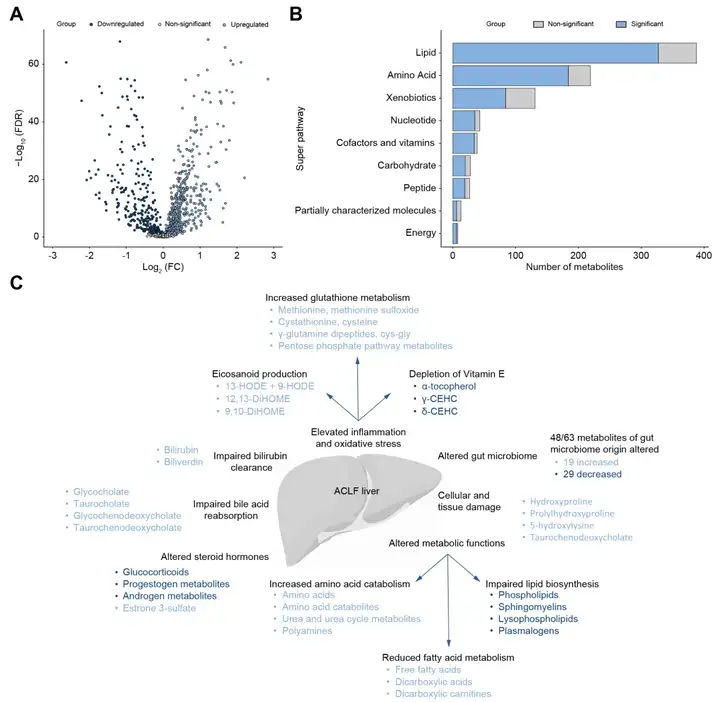
(3)预测HBV-ACLF患者90天死亡率生物标志物的开发和验证
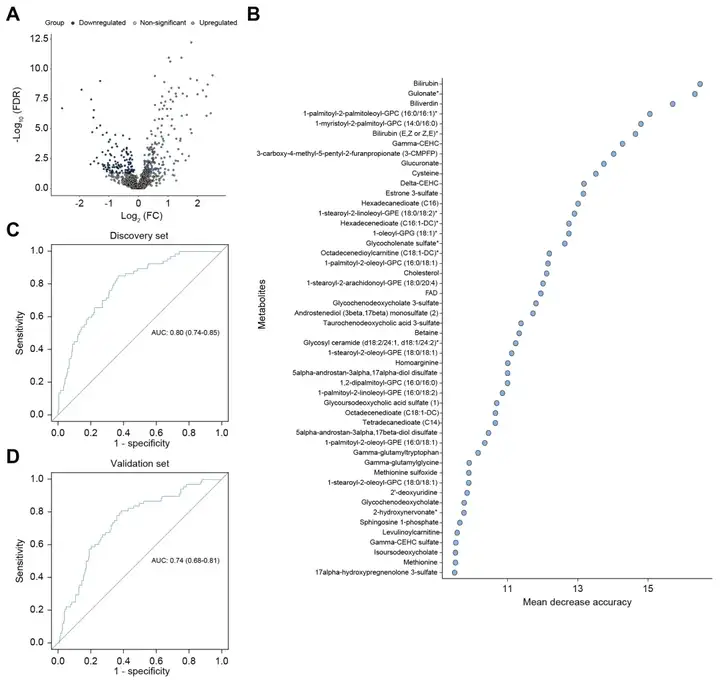
将ACLF样本随机分成相等的两半,作为训练集(120名幸存者和64名非幸存者)和验证集(120名幸存者和63名非幸存者)。非幸存者组和幸存者组共有270种差异代谢物(图8 A),涉及氨基酸降解、脂肪酸ω-氧化、氧化应激途径和激素途径。使用随机森林对代谢物进行排序,结果与错误发现率(FDR)排名最高的代谢物在很大程度上重叠(图8 B)。根据t检验/随机森林排名前50的代谢物进行靶向分析,得到31种差异代谢物,根据逻辑回归模型分析发现哌啶甲酸、NAAG和酰脲丙酸为一个诊断模型,这个模型在发现集和验证集预测ACLF 90天死亡率的曲线下面积(AUC)分别为0.79和0.71(图8 C和D)。
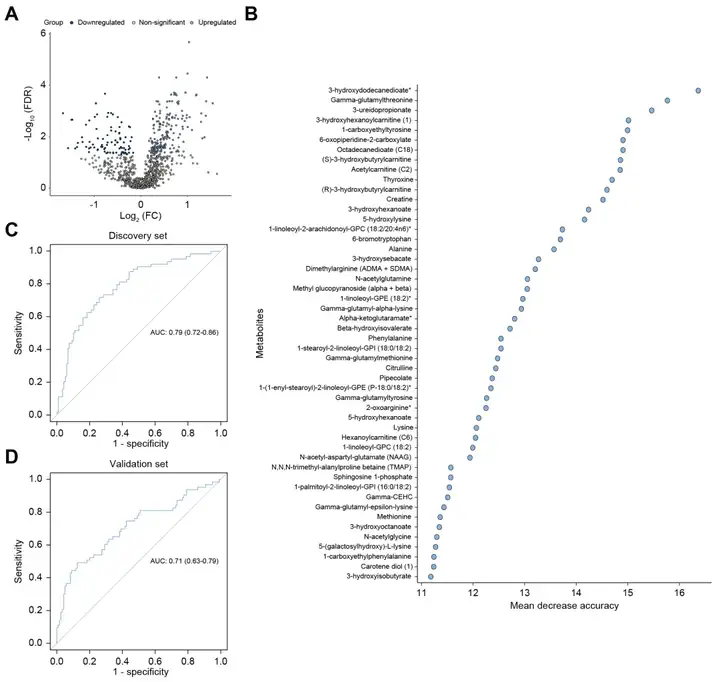
(4)HBV-ACLF诊断前生物标志物的开发和验证
将非ACLF 657例样本随机分成相等的两半,作为发现集和验证集(发现集中包括67个前ACLF样本和261个非ACLF样本,验证集中包括68个前ACLF样本和261个非ACLF样本)。前ACLF组和非ACLF组共有290种差异代谢物(图9 A),涉及脂肪酸ω-氧化、氧化应激途径、胆红素代谢、胆汁酸代谢和类固醇激素途。用类似于鉴定ACLF死亡率生物标志物的方法,发现哌啶甲酸、γ-CEHC为一个诊断模型,这个模型在发现集和验证集预测ACLF诊断前的AUC分别为0.79和0.74(图9 C和D)。
(5)靶向分析和临床试验模型的开发
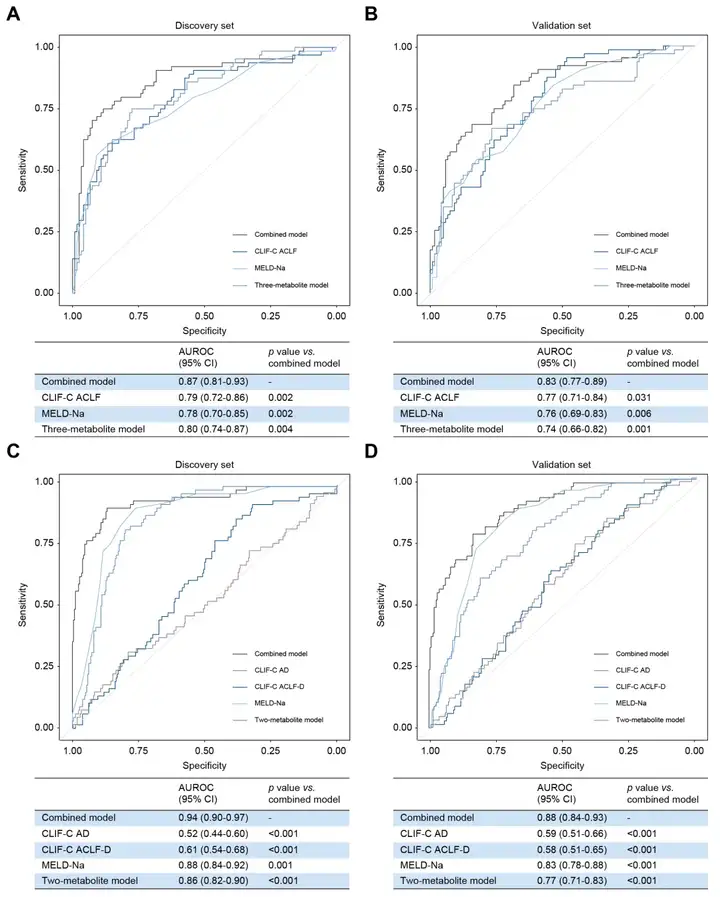
通过LC-MS靶向开发,绝对定量γ-CEHC、NAAG、哌啶甲酸、酰脲丙酸四种标志物。利用三代谢物模型(哌啶甲酸,NAAG,酰脲丙酸)重新评估了ACLF 90天死亡率的预后表现,在该模型中发现集和验证集的AUC分别为0.80和0.74(图10 A和B),高于非靶代谢组学的AUC结果。使用逻辑回归,将临床指标添加到三代谢物模型中,该模型的AUC增加到0.87,高于CLIF-C ACLF、MELD-Na和单独代谢物模型(图10 A),同时在验证集中也得到相同的结论(图10 B)。利用双代谢物模型(哌啶甲酸和γ-CEHC)评估了ACLF诊断前的准确性,在该模型中发现集和验证集的AUC分别为0.86和0.77(图10 C和D)。在模型中加入TB、INR和有无肝硬化指标,最终模型的AUC在发现集中增加到0.94,显著高于CLIF-AD、CLIF-C ACLF-D、MELD-Na和单独的代谢物模型(图10 C),验证集中的也得到了类似的结论(图10 D)。
3、研究结论
本研究通过LC-MS非靶向代谢组学对1024例慢性肝病急性加重患者的血浆进行代谢组学分析,并通过靶向代谢组验证,建立了比现有方法准确性更高的HBV-ACLF早期诊断和预后评估的检测方法。
六、我司优势
1、数据库大:包括Metlin、mzCloud、GNPS、MassBank、HMDB、LipidBlas、Lipidmaps 7大数据库5W+个物质。
2、物质检出数多:项目一般可检出1000-2000种代谢物。
3、分析全面:包括PCA、OPLS-DA、聚类热图、雷达图、VIP值图、火山图、KEGG分析等26项分析内容。
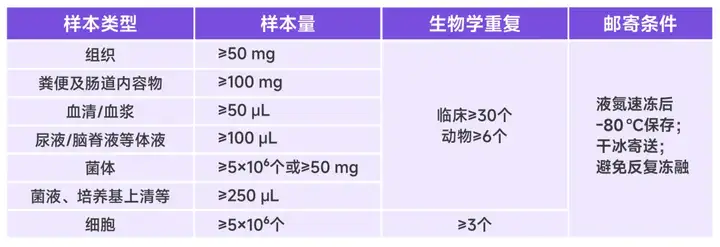
4、分辨率高:基于Orbitrap Exploris 120高分辨质谱仪,可从复杂样品的基质干扰中解析七、样品要求
八、小医叨叨
寻找疾病的生物标志物是代谢组学应用最为广泛的方向之一。代谢物通常可以反映出机体对基因突变及环境影响产生的响应,LC-MS非靶向代谢组学可无偏向地检测样本中能检测到的代谢物分子,通过生信分析进行差异代谢物和通路分析,可寻找疾病的生物标志物,而靶向代谢组可对找到的生物标志物进行验证。所以代谢组学在医学研究领域有重要的价值。我司可提供LC-MS非靶向代谢组学和定制靶向开发服务,为从事疾病的生物标志物研究的科研工作者提供相关服务。
参考文献
[1]Jian G, Tao H.Comparison of Full-Scan, Data-Dependent, and Data-Independent Acquisition Modes in Liquid Chromatography–Mass Spectrometry Based Untargeted Metabolomics[J]. Analytical Chemistry, 2020, 92(12) : 8072-8080.
[2]Yan Z, Wenting T, Xianbo W, et al. Metabolic biomarkers significantly enhance the prediction of HBV-related ACLF occurrence and outcomes[J]. Journal of Hepatology, 2023, 79 : 1159–1171.

