APEX2介导的邻近标记
蛋白质作为生命活动的执行者,机体内各种复杂的生命活动都离不开蛋白间的相互作用,比如信号通路、细胞周期调控、DNA的复制与转录、蛋白质的合成与分泌、信号转导与代谢等,都受到蛋白质等生物大分子间相互作用的严格调控。因此,研究蛋白质与蛋白质之间的相互作用(Protein-Protein Interactions,PPIs)是理解生命活动的基础,鉴定蛋白质与蛋白质之间的相互作用是阐明复杂细胞生理过程分子机制的关键。
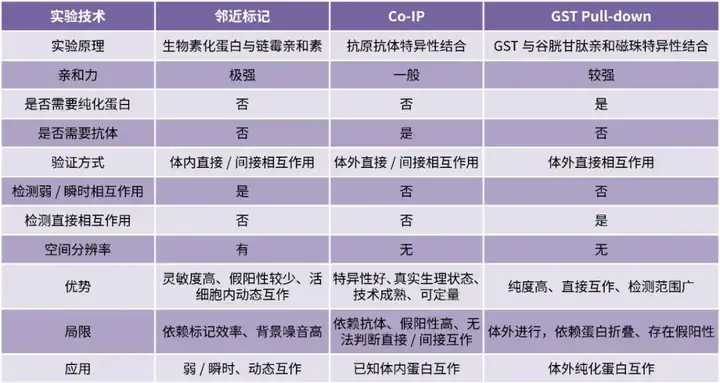
研究蛋白质间相互作用的方法有很多,最经典的就是Co-IP和GST Pull-down。经典就意味着传统,传统就拥有无可避免的痛点。像Co-IP只能验证已知的高亲和力的稳定的蛋白相互作用,而不能检测弱或瞬时的相互作用,同样GST Pull-down只适合体外纯化好的直接的蛋白相互作用,不能研究动态的,也无法反映细胞内真实蛋白相互作用的情况。
而邻近标记技术(Proximity Labeling,PL)的开发,克服了传统方法的固有局限性,为传统方法提供了一种补充方法,用于绘制活细胞分子间相互作用网络图。有关邻近标记技术更多的介绍,详见“邻近标记技术:研究蛋白互作的利器(一)”、“邻近标记技术:研究蛋白互作的利器(二)”及“邻近标记技术:研究蛋白互作的利器(三)”。
一、APEX2邻近标记技术
APEX2(Ascorbate Peroxidase 2),中文名为抗坏血酸过氧化物酶,是基于豌豆(Pea)源或大豆(Soybean)源的抗坏血酸酶经工程改造而来。2012年,美国科学家Alice Ting实验室通过位点突变的方法改造野生型抗坏血酸过氧化物酶(Ascorbate Peroxidase,APX),筛选获得了单体性好、催化活性高的APX(Enhanced APX),即APEX。2015年,该实验室利用酵母表面展示技术进一步对APEX进行改良,得到活性更好的升级版APEX2。APEX2是大豆的抗坏血酸过氧化物酶的进化突变体,底物是一种具有膜渗透性的小分子。因此,通过将APEX2酶与目标蛋白质融合,利用APEX2酶催化底物转化为活性自由基,这些自由基就能够与邻近的蛋白质共价结合,从而实现对邻近蛋白质的标记。而且,APEX2标记时间短,反应速度快,标记反应只需要1min,并可以在1ms以内标记空间范围在20nm以内的蛋白质,基于此特点对瞬时和长时程的生物过程均可进行标记,非常适用在活细胞中研究蛋白质的亚细胞定位、动态迁移以及蛋白质-蛋白质相互作用。此外,APEX与生物素苯酚(Biotin-phenol,BP)在H2O2的催化下生成生物素-苯氧自由基。这些自由基与富含电子的特定氨基酸反应,使生物素共价连接到蛋白质上。由于苯氧自由基的半衰期很短,又不能透过生物膜,所以APEX邻近标记技术对于研究具有膜封闭结构的细胞器蛋白质组具有独特的优势。
二、APEX2邻近标记技术的原理
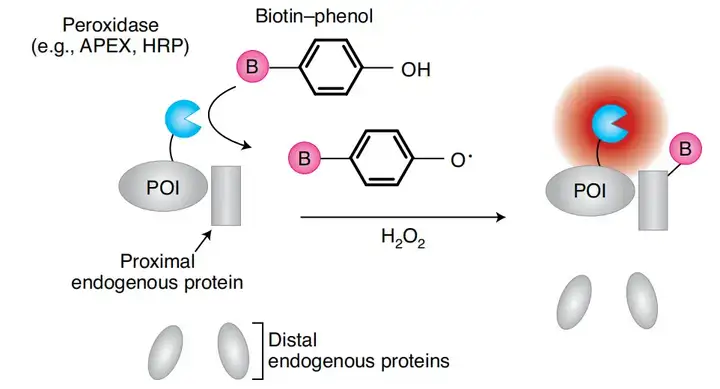
APEX2邻近标记技术的工作原理是将诱饵蛋白与APEX2过氧化物酶融合表达,在H2O2的作用下,APEX2过氧化物酶可催化BP生成生物素偶联的苯氧自由基,产生的生物素-苯氧自由基是短暂的(半衰期<1ms),并且可以共价结合到相邻蛋白质侧链上电子密度较高的氨基酸,如酪氨酸(Tyr)、色氨酸(Trp)、组氨酸(His)和半胱氨酸(Cys),从而使诱饵蛋白的邻近蛋白带上生物素标签。通过偶联链霉亲和素(Streptavidin)的珠子对生物素修饰的蛋白质进行亲和富集,将富集得到的蛋白质经过SDS-PAGE分离,进一步胶内酶解。最后,利用LC-MS/MS方法对生物素修饰的蛋白质进行鉴定,得到诱饵蛋白的邻近蛋白质组。
三、APEX2邻近标记技术的实验流程
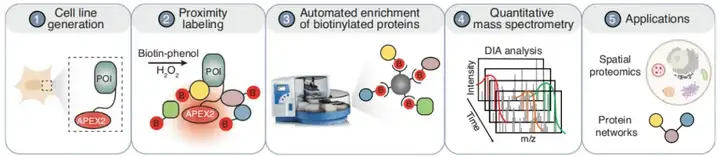
APEX2邻近标记技术的实验步骤与TurboID邻近标记的实验步骤基本相同,但又有些稍微的不同,下面我们看一下APEX2邻近标记操作步骤:
1.构建表达载体
(1)首先需要构建一个包含目的蛋白和APEX2的载体。这个载体用于将APEX2与目标蛋白融合表达,以便进行邻近标记。
(2)确保APEX2的活性位点暴露,以便能够与生物素苯酚反应。
2.转染
(1)将构建好的表达载体转染(如脂质体转染、电穿孔和慢病毒感染等)到宿主细胞或生物体中。
(2)确保目标蛋白-APEX2融合蛋白在宿主中得到充分表达。
3.细胞培养
在适宜的条件下培养细胞,直到融合蛋白的表达达到一定水平。
4.激活APEX2
(1)由于APEX2是一种依赖H2O2激活的过氧化物酶,因此需要在实验中添加H2O2来激活APEX2的过氧化物酶活性。
(2)在细胞培养基中添加适量的H2O2,通常为1mM H2O2,室温孵育1min,以激活APEX2。如有需要也可以对H2O2浓度、标记时间和标记温度等进行梯度摸索,以寻找最适合的反应条件。
5.邻近标记
(1)在APEX2激活后,添加生物素苯酚作为APEX2的底物。建议在5-500μM浓度范围内对生物素衍生物设置梯度。
(2)APEX2将催化生物素苯酚与邻近的蛋白质发生共价结合,形成生物素标记的蛋白质。
6.终止反应
标记完成后,去除H2O2和生物素苯酚,以终止APEX2的活性。
7.细胞裂解
收集细胞并进行裂解,以释放细胞内的蛋白质。
8.生物素标记蛋白的富集
使用链霉亲和素磁珠或琼脂糖珠等亲和素基质,从裂解液中富集生物素标记的蛋白质。
9.蛋白质分析
对富集的蛋白质进行质谱分析,以鉴定与目的蛋白邻近的蛋白质。
10.数据分析
使用生物信息学工具分析质谱数据,确定与目标蛋白相互作用的蛋白质。
11.验证
后续可通过Co-IP、GST Pull-down或酵母双杂等方法验证APEX2邻近标记实验的结果。
注意:实验的具体步骤可能会根据实验目的、所使用的细胞类型、实验条件等因素有所不同。此外,实验操作应遵循实验室安全规程和生物安全指南。
参考文献
Barbara T ,Victoria M ,Kaspar B .In vivo Proximity Labeling of Nuclear and Nucleolar Proteins by a Stably Expressed, DNA Damage-Responsive NONO-APEX2 Fusion Protein[J].Frontiers in Molecular Biosciences,2022,9914873-914873.
Wei Q ,F. K C ,E. P C , et al.Deciphering molecular interactions by proximity labeling[J].Nature Methods,2021,18(2):133-143.
Zhong X ,Li Q ,Polacco J B , et al.A proximity proteomics pipeline with improved reproducibility and throughput.[J].Molecular systems biology,2024,20(8):952-971.

