*仅供医学专业人士阅读参考
在新冠肺炎大流行的最开始,就有一个问题困惑着科学家们。新冠肺炎各种表现中,很常见不规则的血栓凝结和中风,这一问题在无症状患者以及感染后遗症的长新冠中都持续存在。
这事儿挺奇怪。
有科学家猜测,新冠病毒诱发免疫系统的快速反应,伴随而来的炎症导致了血栓和中风,但这说不通,因为感染后导致类细胞因子风暴的病毒并不少,却没有谁能像新冠病毒一样诱发这种程度的血栓。
加州大学旧金山分校的Katerina Akassoglou和Warner Greene有了一个大胆的猜测——说不准血栓对于新冠病毒来说是一种必需的武器,而非仅仅是炎症的结果。新冠病毒进化至此,通过血栓来为自己谋求利益。
这一猜想由一篇《自然》论文证实。
研究者们发现,血栓的主要成分,纤维蛋白,是新冠病毒的重要目标。新冠病毒刺突蛋白会特异性与纤维蛋白结合,激活炎症和氧化应激、促进血栓形成。不仅如此,纤维蛋白还会抑制自然杀伤细胞(NK细胞),削弱其杀伤新冠病毒的能力。
结合研究者们之前的工作成果,纤维蛋白会刺激小胶质细胞过度活化,导致后续的神经炎症和神经元丢失,这一过程独立于新冠病毒脑部感染和肺部免疫,研究者认为是新冠肺炎和长新冠中脑雾等神经系统症状的罪魁祸首。
这一研究颠覆了此前新冠肺炎血栓的认知,强调了血栓在炎症、病毒清除障碍以及新冠肺炎和长新冠常见神经系统症状中的作用。
论文题图
血栓在新冠感染者中相当常见,轻度感染、突破性感染、长新冠、年轻患者中均有报告,且与神经系统并发症有关。有研究发现,新冠肺炎导致的血栓异常“顽固”,抗凝治疗都不能完全对付。
结合前文,可见新冠肺炎血栓相当特殊。
研究者们猜测,新冠病毒或许能够直接作用于纤维蛋白,不仅促进血栓形成,还一定程度上改变了血栓的结构和功能。
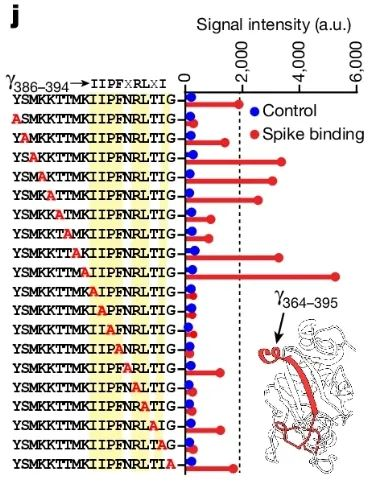
实验结果显示,虽然亲和力不如ACE2,但纤维蛋白的确能够与刺突蛋白结合。结构上,纤维蛋白的γC结构能与刺突蛋白相应表位结合,激活先天免疫反应。
纤维蛋白和刺突蛋白的部分结合表位
纤维蛋白与刺突蛋白共孵育显著延迟了纤维蛋白的溶解,与此前对新冠患者血栓的研究结果一致。刺突蛋白会显著增强纤维蛋白诱导的骨髓来源的巨噬细胞(BMDM)的活性氧(ROS)释放,也就是说新冠病毒增强了纤维蛋白诱导的炎症。
小鼠实验显示,新冠病毒感染通过纤维蛋白信号诱导炎症细胞浸润、氧化应激和纤维化,这一过程由CD11b-CD18介导。敲除小鼠纤维蛋白或令其失去CD11b-CD18结合基序,小鼠感染新冠病毒后的巨噬细胞浸润和肺部胶原蛋白沉积等病理都显著减弱。
有趣的是,研究者分析这些小鼠感染后肺部转录组变化的时候,发现缺失纤维蛋白的小鼠中,NK细胞相关的表面抗原编码基因Klrb1a等发生了显著变化,这意味着纤维蛋白还具有调节NK细胞功能的作用。
NK细胞是清除病毒的重要细胞,有研究显示NK细胞募集和活化的削弱与新冠肺炎不良结局有关。
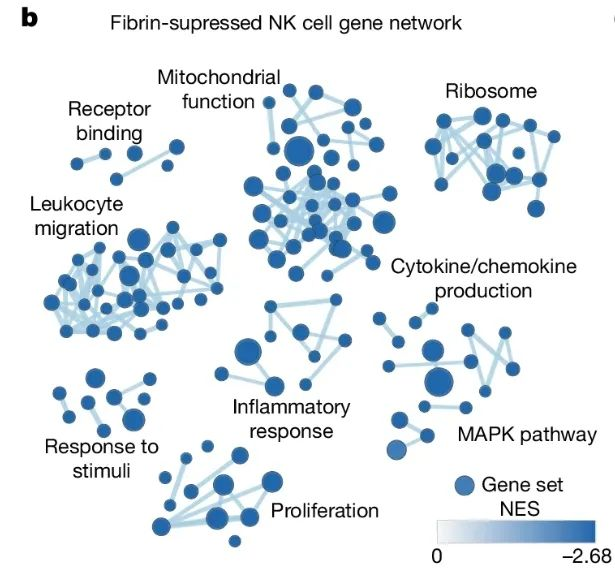
RNA测序结果显示,纤维蛋白会显著抑制一系列基因表达,包括线粒体功能、白细胞迁移、细胞因子/趋化因子产生、炎症反应、增殖等等。纤维蛋白会下调JAK-STAT通路和p38 MAP激酶的多个靶标,削弱NK细胞活化。
纤维蛋白抑制了NK细胞中的多个通路
纤维蛋白的作用并不依赖于新冠病毒感染。研究者给小鼠注射了含有刺突蛋白的假病毒,发现这依旧能够诱导氧化应激和肺部的纤维蛋白沉积。在纤维蛋白诱导的脑脊髓炎小鼠中,注射刺突蛋白也会加剧小胶质细胞反应性。
也就是说,在没有活动性感染的情况下,纤维蛋白+刺突蛋白的组合依旧会引发炎症和氧化应激,长新冠或许就是这么来的。
既然如此,纤维蛋白就成了治疗长新冠炎症和保护神经的有潜力靶点。
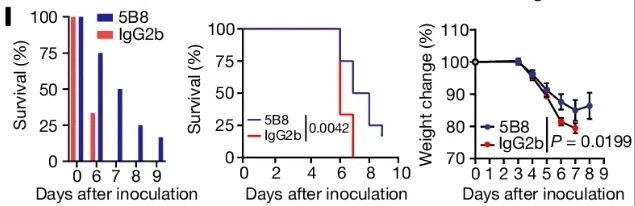
研究者测试了一种针对纤维蛋白炎症结构域的单克隆抗体5B8。在小鼠中,预防性施用5B8能够显著减少新冠病毒感染导致的巨噬细胞活化、氧化应激、胶原蛋白积累、纤维蛋白沉积,同时促进了肺部的NK细胞反应。感染后24小时给予5B8治疗,也能显著减少巨噬细胞活化和氧化应激。
对Delta毒株感染也有效果
5B8已经进入1期临床试验。纤维蛋白在多发性硬化症、阿尔茨海默病(AD)等疾病中都有病理作用,该药物有望用于相关治疗。此前的实验中,消除纤维蛋白炎症结构域可保护AD小鼠免遭突触丢失和认知障碍。
虽然新冠大流行已经过去,但全球范围内仍有数亿人被长新冠困扰。希望有效的解决办法能够早点出现。
参考资料:
[1]https://www.nature.com/articles/s41586-024-07873-4
[2]https://www.sciencedaily.com/releases/2024/08/240828114448.htm