*仅供医学专业人士阅读参考
Tau蛋白病与Tau蛋白异常磷酸化积累有关,患者活性氧(ROS)水平异常升高。
神经元对高水平ROS异常敏感,会产生脂质过氧化物以减少神经元内部的ROS。这些被排斥的脂质过氧化物由载脂蛋白转移至胶质细胞,并整合到脂滴(LD)中,再进一步被氧化分解。LD形成缺陷与阿尔茨海默病(AD)风险有关。
近日,来自贝勒医学院研究人员在《自然·神经科学》杂志上发表了最新研究成果,首次证实了Tau蛋白可以通过调节神经胶质细胞LD形成来抵抗ROS损伤。
研究发现,Tau蛋白过度积累会影响LD形成,使神经元中毒性脂质过氧化物水平升高。但是正常LD的形成离不开内源性Tau的存在,Tau蛋白缺失的果蝇出现退行性表型,寿命缩短,运动能力下降。

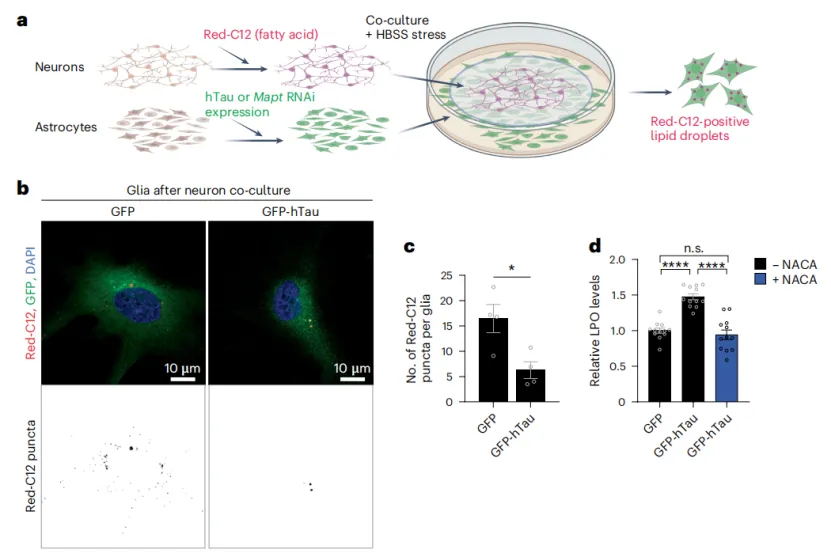
研究人员首先在果蝇中讨论了Tau蛋白积累对LD形成的影响。通过在视网膜胶质细胞中过表达人源Tau蛋白,研究人员并没有观察到LD水平增加,相反,LD数量减少了76%-91%。同时,因为LD形成受限,毒性脂质过氧化物的水平增加了一倍还多(113%)。
Tau过表达导致LD数量减少了和LPO水平升高
但是,如果Tau完全消失,也不是什么好事。研究人员构建了Tau蛋白功能丧失的果蝇模型,不仅LD数量减少,神经胶质细胞也受到显著影响,体积迅速增大,长期暴露于ROS还会出现显著退化和破碎,空泡取代了正常的细胞组织。说明Tau蛋白缺失使胶质细胞更容易受到ROS伤害。
很明显,Tau蛋白功能丧失导致了LD介导的脂质代谢缺陷,不仅脂质过氧化物水平升高,还出现了甘油三酯累积,果蝇睡眠也受到影响,表现为白天的睡眠时间增加了107%。此外,Tau蛋白功能丧失使果蝇的运动能力下降,寿命缩短。
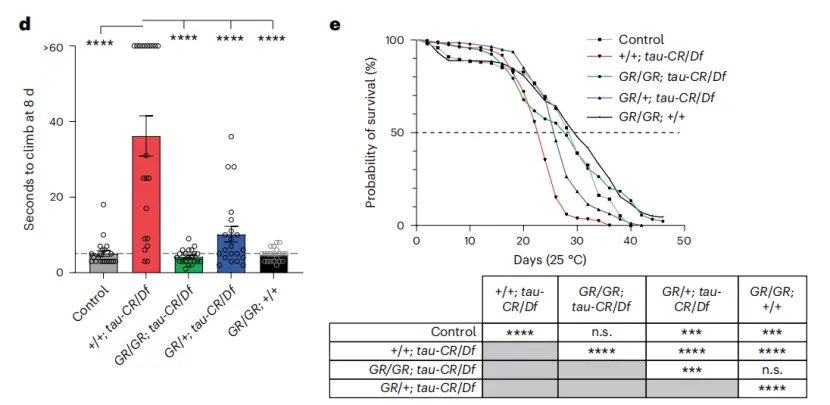
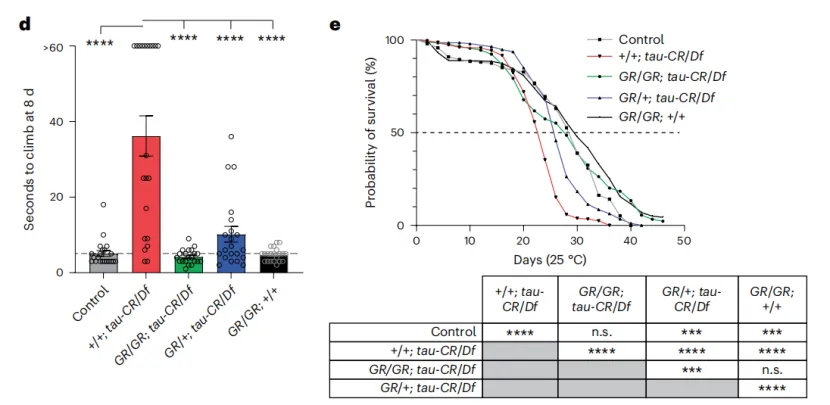
Tau缺失果蝇运动能力和寿命受损
诚然,补充Tau蛋白或者恢复Tau功能可以挽救果蝇的运动缺陷和部分存活率。但是经过实验,研究人员发现恢复LD形成就可以缓解果蝇的运动缺陷,说明运动缺陷出现的根本原因还是Tau蛋白缺失造成LD形成受损。
既然这样,那么Tau蛋白过度表达的相关影响也就可以理解了。LD形成是一个高度保守的过程,高水平的Tau蛋白积累会干扰ROS环境下的LD形成,导致LD数量减少和脂质过氧化物水平升高,进而出现退行性表型。
应激条件下,Tau蛋白积累导致LD数量减少
接下来,研究人员评估了大鼠内源性Tau在LD形成中的作用。在非氧化应激条件下,Tau缺失大鼠可以正常形成LD,但是在应激条件下,Tau缺失大鼠的LD数量显著降低,脂质过氧化物水平升高,说明内源性的Tau缺失影响了大鼠神经细胞在应激条件下的自我保护能力。
为了研究LD负荷与疾病之间的关系,研究人员分析了Tau蛋白编码基因MAPT和LD标记物PLIN2在老年人类大脑中的表达。结果显示,MAPT和PLIN2的表达存在显著负相关,但是这一关联与阿尔茨海默病的临床诊断无关,而是在老年人中普遍存在。
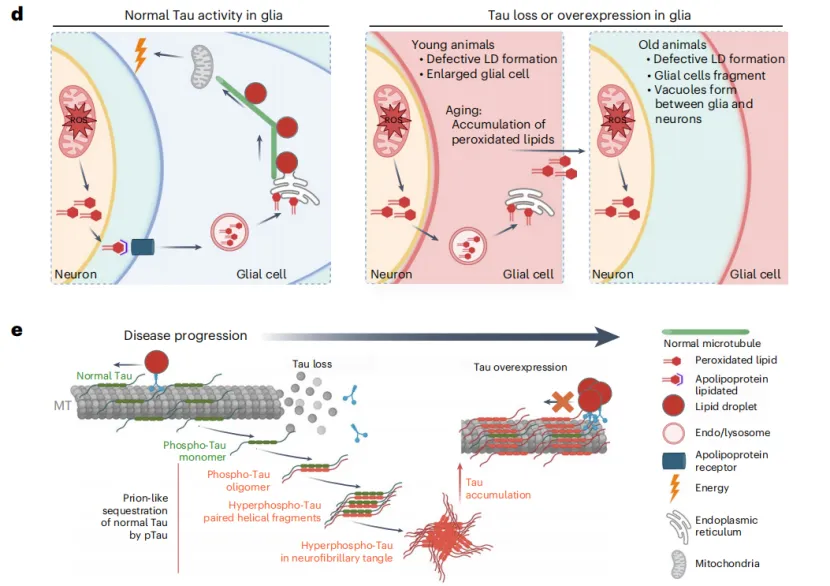
总的来说,研究证明,LD形成是机体应对ROS的自我保护机制,Tau的过度积累或缺失都会影响胶质细胞形成LD的能力,导致脂质过氧化物水平升高,进而影响运动能力和寿命。研究揭示了Tau在脂质代谢中的重要调节作用,表明针对Tau的治疗方式需要区分正常的内源性Tau蛋白和过度的Tau积累。
参考文献:
Goodman L D, Ralhan I, Li X, et al. Tau is required for glial lipid droplet formation and resistance to neuronal oxidative stress[J]. Nature Neuroscience, 2024: 1-16.
文章来源:奇点神思

