阿尔茨海默病(AD)难以攻破,其复杂的病理和难解的病因要担一份责任。
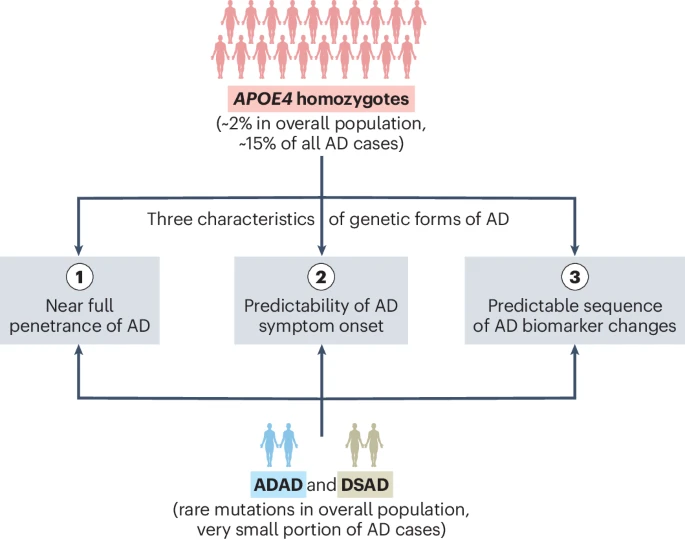
AD的发病涉及颇多遗传变异,第一档要数APP、PSEN1和PSEN2三个基因,这三者的突变会导致早发性常染色体显性遗传性阿尔茨海默病(ADAD);其次是唐氏综合征带来的APP基因多拷贝,由此发展为唐氏综合征相关的阿尔茨海默病(DSAD)。
在这两种遗传性AD之外,散发性/迟发性AD占了病例中的更多数,与之相关的风险基因也有数十个之多,其中风险最高的莫过于APOE4基因。
今日,来自西班牙的科学团队在《自然·医学》发文,研究者们提出,APOE4不应当仅被视为AD的风险基因,而是应当被认定为AD的致病基因。APOE4纯合完全满足遗传性AD的三大主要特征,即近乎完全的疾病外显率、症状发作年龄的可预测性、病理/生物标志物/临床表现的可预测变化。
考虑到APOE4纯合在全球人口中高达2%的流行率,APOE4遗传性AD或将一跃成为最常见的单基因遗传病之一。
而将APOE4视为AD的致病基因,这无论是对AD的诊断治疗,还是临床药物的研发与试验设计,都会产生巨大的影响。
其实,APOE4早就表现出了与其他风险基因不同的“风采”。
APOE4纯合者患AD痴呆风险,在85岁时可高达60%,远高于杂合携带者或非携带者。这一数值也与其他全基因组关联研究发现的低风险基因并不匹配,已经达到了孟德尔遗传病(即单基因遗传病)的量级。
研究者调取了来自美国国家阿尔茨海默病协调中心(NACC)的3297名捐献者的脑病理数据,以及其他5个已发表的大型多中心AD生物标志物队列研究的10039人数据,对其中APOE4相关内容进行了分析。
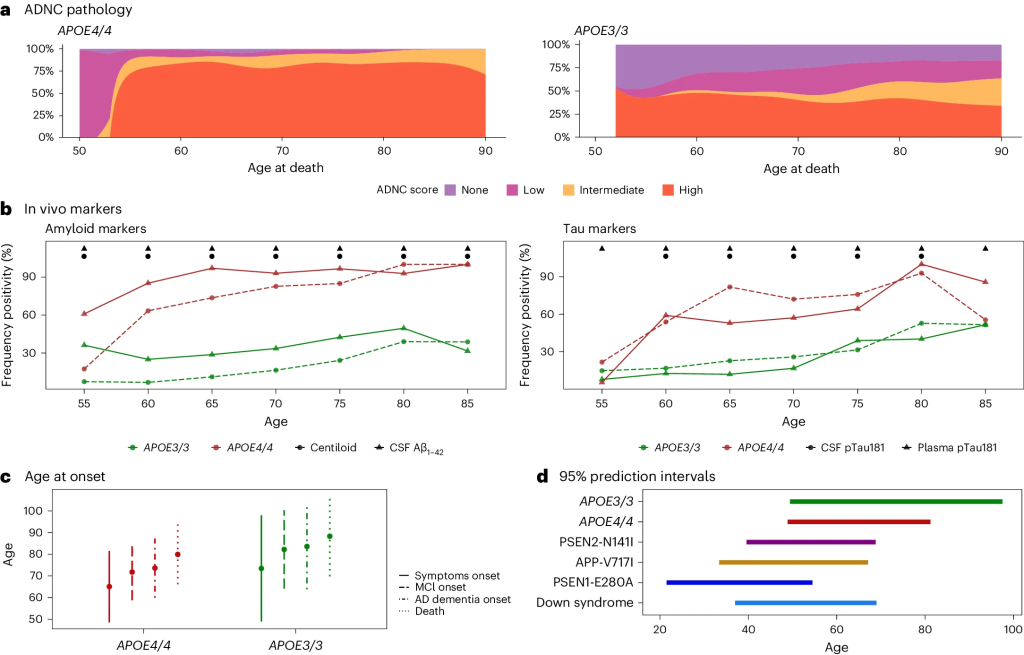
生物标志物分析结果显示,几乎所有的APOE4纯合者都表现出了高或中的阿尔茨海默病神经病理学变化评分(ADNC),而APOE3纯合者中仅有50%符合这一情况。此外,无论死亡时年龄如何,APOE4纯合者的神经病理学结果都是一致的。
针对脑脊液Aβ42、脑脊液pTau181的进一步分析显示,从55岁开始,APOE4纯合者体内的生物标志物水平始终高于APOE3纯合者;到65岁时,几乎所有APOE4纯合者都表现出异常的脑脊液Aβ42水平、PET呈淀粉样蛋白阳性;80岁时,生物标志物外显率达到88%。
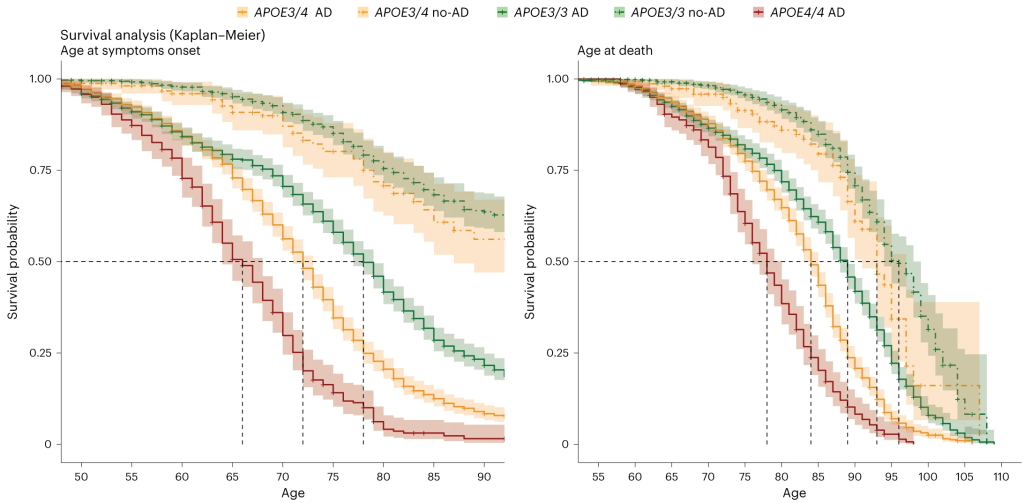
对疾病进展阶段的分析显示,APOE4纯合者约在65.6岁时开始出现AD症状,71.8岁时出现轻度认知障碍(MCI),73.6岁进展为痴呆,77.2岁死亡,比APOE3纯合者早约7-10年。
Kaplan-Meier生存分析显示,APOE4对发病年龄和死亡年龄具有显著的剂量效应。
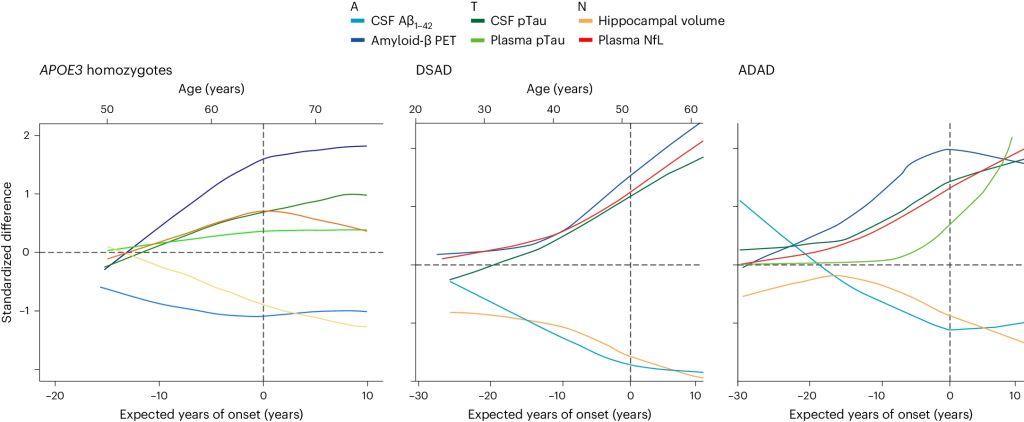
分析生物标志物变化自然史也可以发现,APOE4纯合者与ADAD和DSAD存在时间的相似性。
此外,APOE3/4杂合无论生物外显率、认知改变年龄、临床表现还是生物标志物变化,表型始终介于APOE3纯合和APOE4纯合之间,强调了APOE4的剂量效应。
综上,APOE4已经完全满足了遗传性阿尔茨海默病的三大主要特征——近乎完全的疾病外显率、症状发作年龄的可预测性、病理/生物标志物/临床表现的可预测变化。
与此形成呼应的是,前段时间发表在《神经元》杂志上的一项研究也发现,APOE4通过异常功能的获得驱动AD,并支持了将APOE4的沉默或敲除作为一种可行的治疗方案。
将APOE4重新定义为AD的致病基因,将对AD的研究产生巨大的影响。APOE4在AD发展中究竟扮演什么样的角色会成为今后研究的重点,直接靶向APOE4的新药也将被纳入视野,基因疗法和细胞替代疗法潜力大增,临床试验设计也需要格外考虑APOE基因型分组。
参考资料:
[1]https://www.nature.com/articles/s41591-024-02931-w
[2]https://www.nature.com/articles/s41591-024-02923-w
文章来源:奇点网