我相信,很多人都经历过在出远门前、大型考试前、工作完不成等各种各样压力贼大的时候,不仅心里揪揪着,肚子也开始莫名其妙地抽抽
压力,你祸祸脑子、发量就够了,怎么还要拧巴肠道啊!
近日一篇发表在顶刊《细胞》上的文章,可算给出了答案。
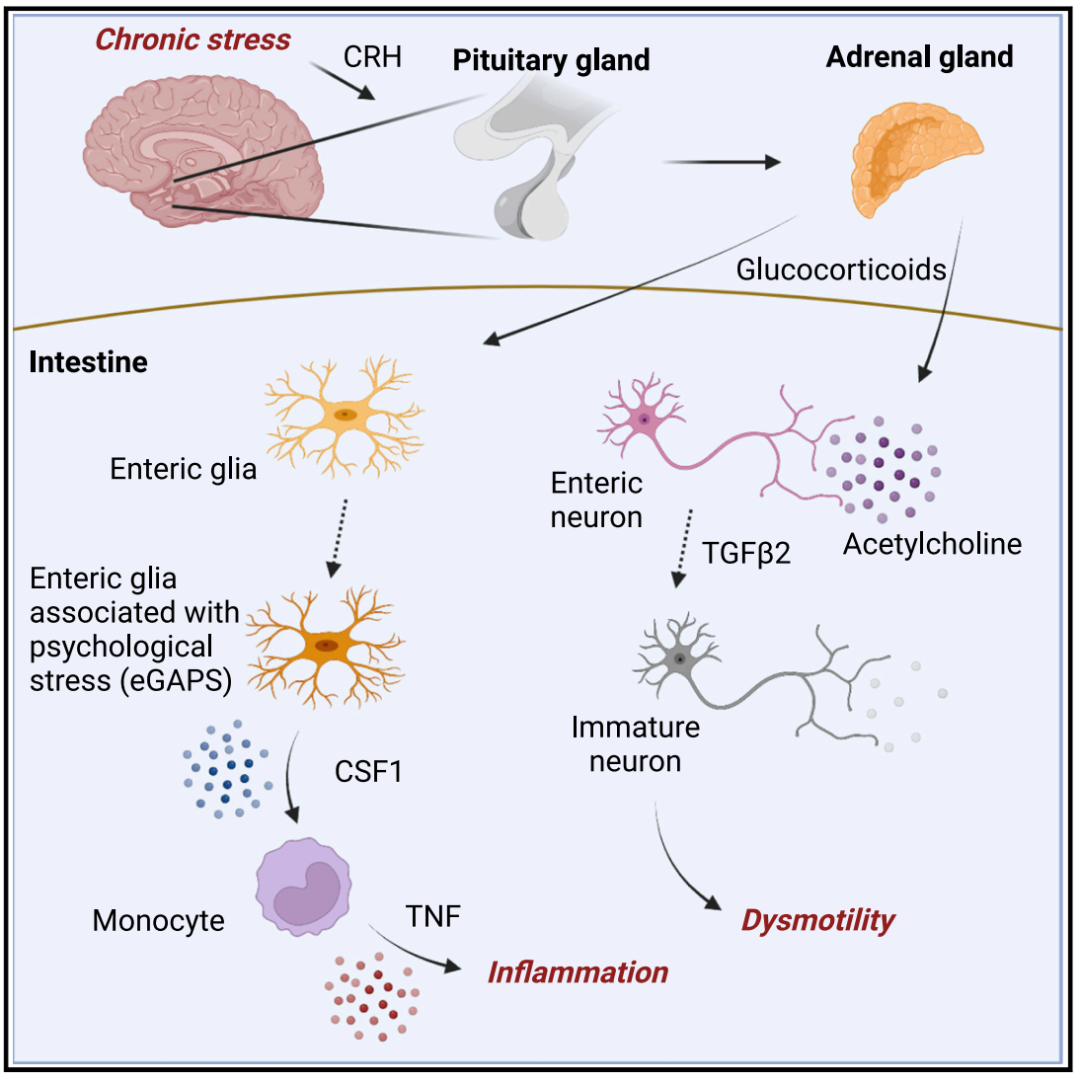
美国宾夕法尼亚大学的Christoph A. Thaiss和Maayan Levy及其同事们发现,肠道神经系统是连接心理压力与肠道炎症的关键一环。长期心理压力导致的糖皮质激素水平持续升高,一方面会引起肠道神经胶质细胞发生转变,进而导致炎症相关的免疫细胞聚集;另一方面还会阻止未成熟的肠道神经元充分发育,引起肠道蠕动障碍[1]。
论文首页截图
炎症性肠病(IBD)属于慢性炎症性肠道疾病,表现为肠道黏膜的持续或反复炎症,从而导致肠道组织受损和功能障碍。炎症性肠病主要包括克罗恩病和溃疡性结肠炎,常见症状有腹痛、腹泻、疲劳、消化道或直肠出血等。
炎症性肠病的发病机制尚不完全清楚,可能与遗传因素、免疫系统异常、环境因素和肠道菌群紊乱等因素有关。而越来越多的流行病学研究指出,心理压力会给肠道炎症火上浇油,但这其中缘由也未揭示。
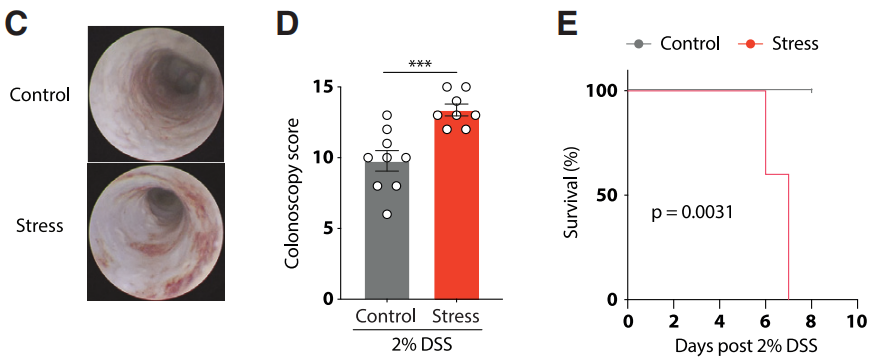
在这项研究中,Christoph A. Thaiss和Maayan Levy等人首先利用多种小鼠模型发现,心理压力确实会加剧肠道炎症。尤其是在肠道炎症开始发作前这个时间点施加压力,可以达到最强的病情加重效应。但是,心理压力本身却不足以引起小鼠明显的肠道炎症。
这些说明,心理压力可能使肠道预先处于炎症状态,从而在接触到肠道炎症诱发因子后放大炎症反应。
有心理压力的小鼠肠道炎症病情更严重
使用单细胞RNA测序、流式细胞术等技术,研究者们发现心理压力加剧肠道炎症的效应是由肠道中的单核细胞所介导。
当小鼠处于心理压力下时,分泌炎症因子TNF的单核细胞大量积累,构成炎症环境。如果使用单克隆抗体药物抑制单核细胞上TNF的表达,便可以抵消心理压力对肠道炎症的影响。
那么,心理压力究竟是如何从大脑传递到远处的肠道呢?
中枢神经系统在感知到压力后,能够诱发外周神经系统中儿茶酚胺和糖皮质激素水平升高[2]。在这里,研究结果显示,儿茶酚胺对肠道起到的是保护作用,减少儿茶酚胺会帮倒忙,导致小鼠发生严重的肠道黏膜损伤、体重减轻和死亡率提升。相反,降低糖皮质激素水平或抑制其介导的信号通路,才是缓解小鼠肠道炎症的正解。
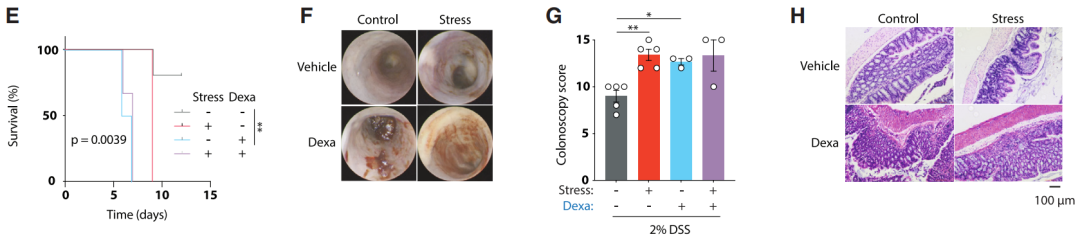
而如果长期使用药物(地塞米松)治疗给小鼠补充糖皮质激素,则会引发与刚才观察到的由心理压力带来的相似效应,导致小鼠肠道炎症的病情加剧,以及召集单核细胞。
以上结果表明,糖皮质激素正是压力祸祸肠道免疫细胞的手段。
药物治疗使糖皮质激素升高,可以“复刻”心理压力对肠道炎症的影响
不过,事情还没有这么简单,中间夹着一个关键的“中介人”——肠道神经系统。
研究者们起初认为,糖皮质激素是直接“迫害”肠道中的免疫细胞,通过与单核细胞上表达的相应受体结合来达到其目的。结果却显示,即使小鼠肠道内单核细胞上不表达糖皮质激素的受体,心理压力照样能够加剧肠道炎症。换句话说,糖皮质激素的直接下线不是单核细胞。
于是,研究者们想到了肠道里的神经系统。
他们发现,肠胶质细胞的存在及其正常表达的糖皮质激素受体,是心理压力加剧小鼠肠道炎症、单核细胞聚集的必要因素。
不仅如此,利用聚类分析等方法,研究者们抓住一群鬼鬼祟祟的肠胶质细胞。这些细胞具有相同的基因表达谱,以促炎和促凋亡信号通路上调、调节细胞之间相互作用的信号通路下调为特征,且仅在小鼠处于心理压力之下或者糖皮质激素水平升高时才会现身。
有个肠胶质细胞亚群形迹可疑
随后的研究结果摸清了具体机制。在漫长的心理压力煎熬下,肠胶质细胞长期暴露于高水平的糖皮质激素。糖皮质激素与其表达的相应受体结合后,诱导它们也发生“心态上的转变”,成为心理压力相关肠胶质细胞(eGAPs)。eGAPs会分泌一种称为CSF1蛋白的细胞因子,进而促进分泌炎症因子的单核细胞聚集,为肠道的炎症环境添一把大火。
肠道此时欲哭无泪,你大脑过得不好就算了,还来搞我家神经系统的心态。不过这不算完,糖皮质激素藏着另外一手。
咱总说,压力大,长不高。确实如此啊,研究者们发现,糖皮质激素会“压迫”肠道神经元的发育。
在心理压力下或使用药物补充糖皮质激素时,肠道内不成熟的神经元占比明显增加、成熟神经元减少,并且重要的神经递质乙酰胆碱水平下降。肠道神经元的发育不良,进一步导致了小鼠肠道功能异常,比如食物移动缓慢、便秘等,最终增加肠道炎症的不适感。
心理压力祸害肠道神经系统的机制图
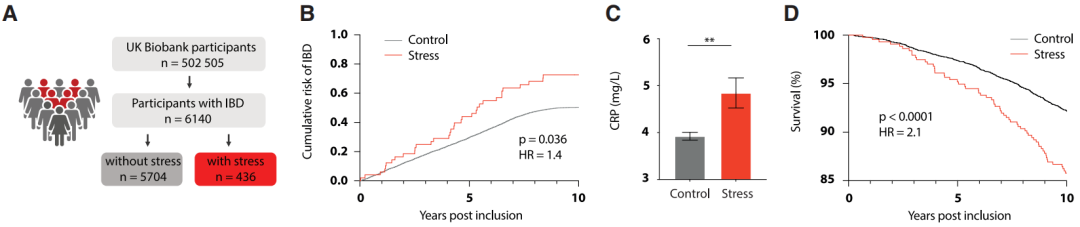
最后,研究者们利用来自英国生物库的502505个人的数据以及其他队列的数据进行分析发现,与没有心理压力相比,长期处于较大心理压力的人在10年内发展为炎症性肠病的风险更高。而且,心理压力与患者病情严重程度以及肠道内单核细胞聚集、TNF等炎症标志物水平呈正相关。
大型队列研究结果验证了心理压力与肠道炎症之间的关联
总而言之,这项研究实锤了心理压力与肠道炎症之间的关联,发现在长期心理压力下,持续升高的糖皮质激素会重创肠道神经系统,营造肠道炎症环境和阻碍肠道蠕动。
令研究者们不解的是,在炎症性肠病患者的临床治疗中,常使用到糖皮质激素药物泼尼松来抗炎、抗过敏,这与研究结果相悖。他们猜测,糖皮质激素究竟扮演什么角色,可能与其水平是短暂提升还是持续提升相关。毕竟临床观察结果显示,只有短期治疗才对炎症性肠病有益[3,4],而且在此次研究中使用的糖皮质激素药物地塞米松更加强效、治疗时间也较长。
参考文献:
[1]https://www.cell.com/cell/fulltext/S0092-8674(23)00475-0
[2]Russell, G., and Lightman, S. (2019). The human stress response. Nat.Rev. Endocrinol. 15, 525–534. https://doi.org/10.1038/s41574-019-0228-0.
[3]Bruscoli, S., Febo, M., Riccardi, C., and Migliorati, G. (2021). Glucocorticoid therapy in inflammatory bowel disease: mechanisms and clinical practice. Front. Immunol. 12, 691480. https://doi.org/10.3389/fimmu.2021.691480.
[4]Waljee, A.K., Wiitala, W.L., Govani, S., Stidham, R., Saini, S., Hou, J., Feagins, L.A., Khan, N., Good, C.B., Vijan, S., et al. (2016). Corticosteroid use and complications in a US inflammatory bowel disease cohort. PLoS One 11, e0158017. https://doi.org/10.1371/journal.pone.0158017.
文章来源:奇点网