譬如,AD的主要病理表现之一,β淀粉样蛋白(Aβ)沉积并不一定会导向tau病理和临床进展。诸多的生物标志物研究标明,在认知未受损(CU)的个体中,Aβ先于tau沉积,这与认知症状的发展密切相关。但是部分个体却能在Aβ病理存在的情况下持续保持认知,并最终不发展为AD。
我们到底忽略了其中的哪个环节?
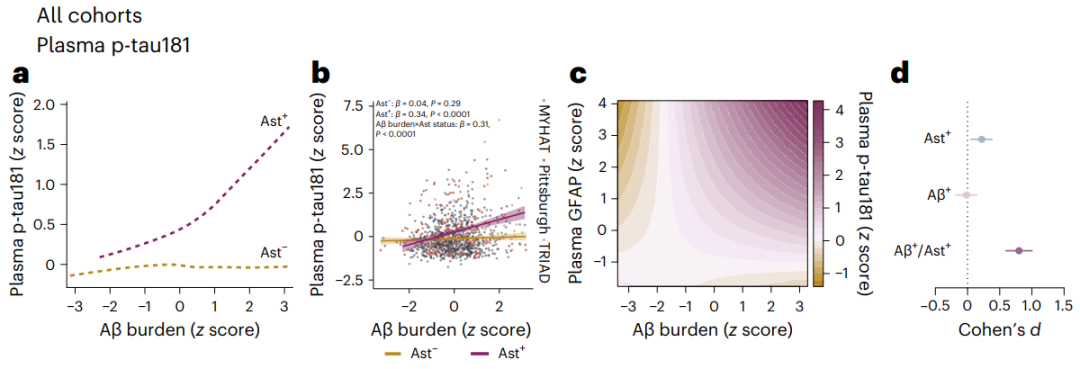
今日,《自然·医学》杂志发表了匹兹堡大学科研团队的最新研究成果。科学家们分析了3个队列的一千余名认知未受损参与者的生物标志物数据,发现了一个重要的事实——Aβ病理会否导向tau病理,要取决于星形胶质细胞状态。仅在星形胶质细胞反应性(Ast)个体中,Aβ负荷与血浆磷酸化tau以及tau缠结存在函数关系。
这项研究结果表明,星形胶质细胞反应性是将Aβ与tau病理的发展联系起来的重要上游事件,将星形胶质细胞反应性标志物纳入临床前AD的分类或许对寻找AD的干预窗口具有重要意义。
尸检研究显示,星形胶质细胞反应性(Ast)是认知未受损个体中常见的神经病理学表现,而且与出现于皮质的Aβ斑块一样,是AD最早出现的异常病理之一。
有研究表明,星形胶质细胞反应性对于触发Aβ诱导的tau磷酸化至关重要,抑制星形胶质细胞反应性能够减轻tau病理;神经胶质纤维酸蛋白(GFAP)阳性的星形胶质细胞能够内化tau,并可能有助于tau复制。
这些研究结果都支持Aβ、星形胶质细胞反应性和tau病理之间存在某种联系。
为了进一步验证这个假设,研究者们利用TRIAD、匹兹堡队列和MYHAT 3个队列研究的数据,分析了Aβ负荷、磷酸化tau/tau缠结与Ast之间的关系。
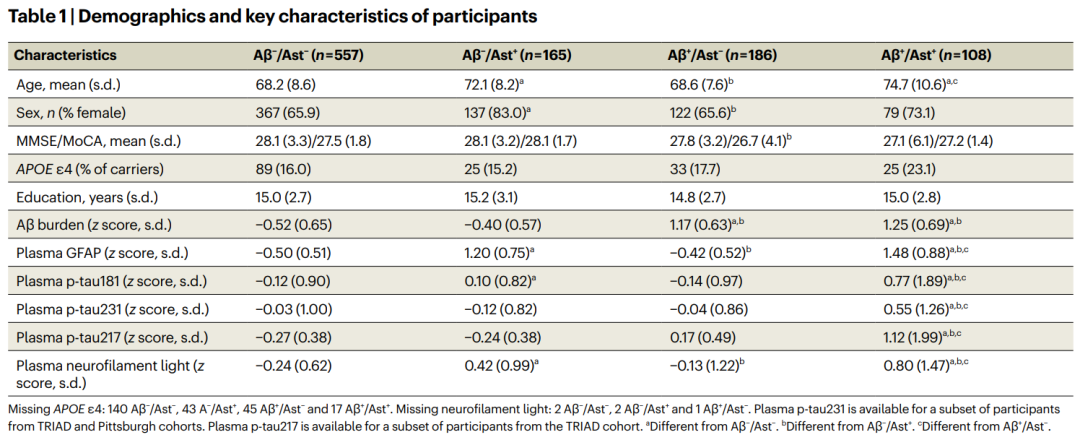
从3个队列中,研究者共选取了1016名认知未受损的个体,平均年龄69.6±8.9岁,CDR评分=0。血浆GFAP与脑脊液(CSF)水平相关,因此基于血浆GFAP水平判断星形胶质细胞反应性阳性与否。此外,3个队列都留存数据的磷酸化tau蛋白标志物仅有p-tau181,因此将p-tau181作为主要分析对象。
总体来说,被分类为Aβ+/Ast+的参与者血浆p-tau181、p-tau231、p-tau217相较其他组更高。而Aβ+/Ast+和Aβ+/Ast–两组之间Aβ水平并无差异。
在3个队列中分别进行同样的分析,结果也是一致的,且没有观察到APOE4状态的影响。
值得注意的是,Ast状态并未影响到任何队列中Aβ负荷与神经丝轻链水平之间的关联,说明星形胶质细胞反应性参与Aβ病理对tau病理的影响,但不参与神经变性。
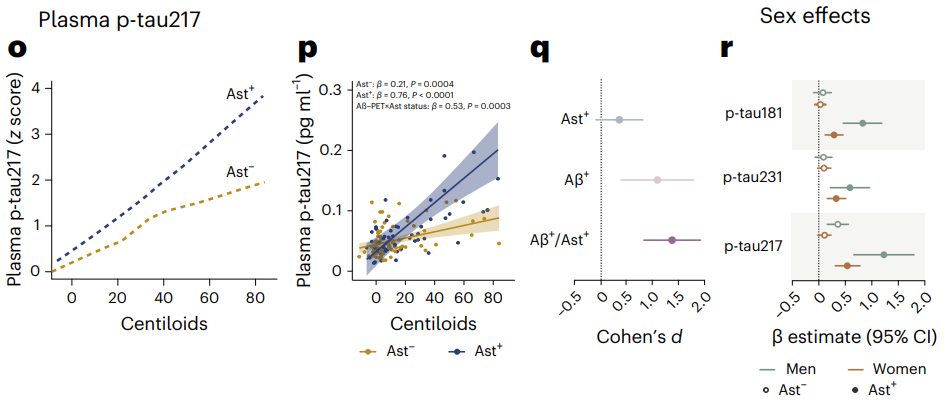
研究者进一步分析了这一过程中的性别差异。有意思的是,男性Ast阳性个体中,Aβ负荷与血浆p-tau相关性更高。
男性中Aβ与tau相关性更强(右)
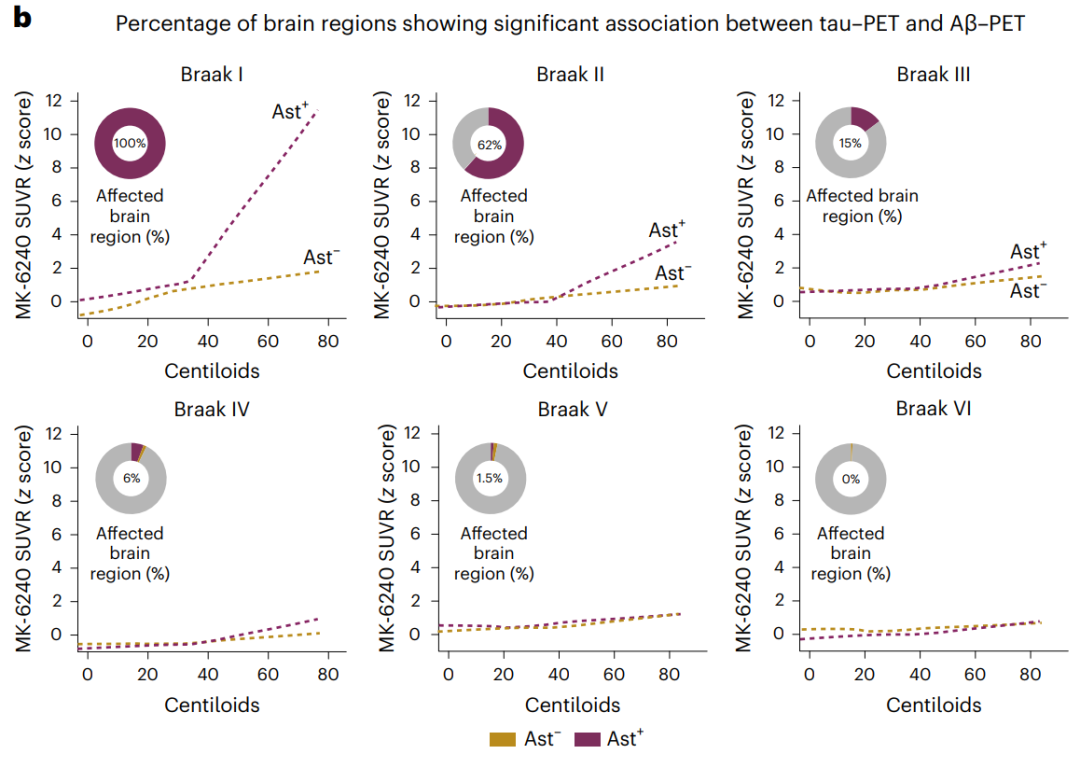
在Ast阳性个体中,PET检测的tau缠结年积累率更高,且可以通过基线Aβ负荷预测。