有句话叫癌症不可怕,转移才可怕。确实,在癌症造成的死亡中,约90%都来自转移癌,也因此,如果能够抓住转移癌的踪迹、尽早治疗,一定能够大大提升癌症患者的生存体验。
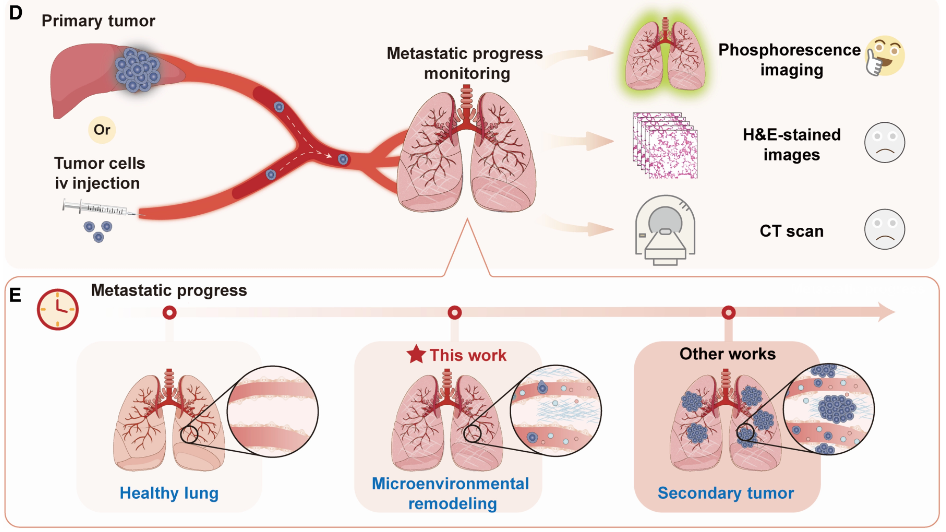
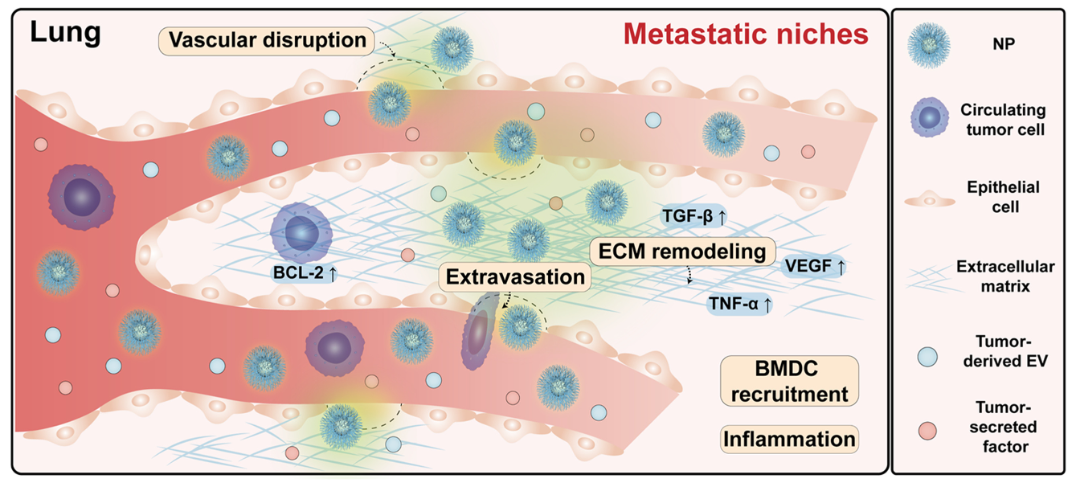
这并不需要等到转移癌产生才能实现。实际上,在癌细胞来到远端器官之前,微环境已经开始默默改变,包括血管渗漏、成纤维细胞改变、髓系细胞募集等等,形成更有利于循环肿瘤细胞(CTC)生长和存活的土壤。
近期,武汉大学李振/李倩倩/张玉峰联合团队在《科学·进展》杂志发表论文,他们设计了一种有机室温磷光纳米颗粒,它能简单安全有效地在体内成像,指示肺部转移前微环境,效果远超现有技术,有望用于转移过程的监测,实现早期诊断和治疗。
论文题图
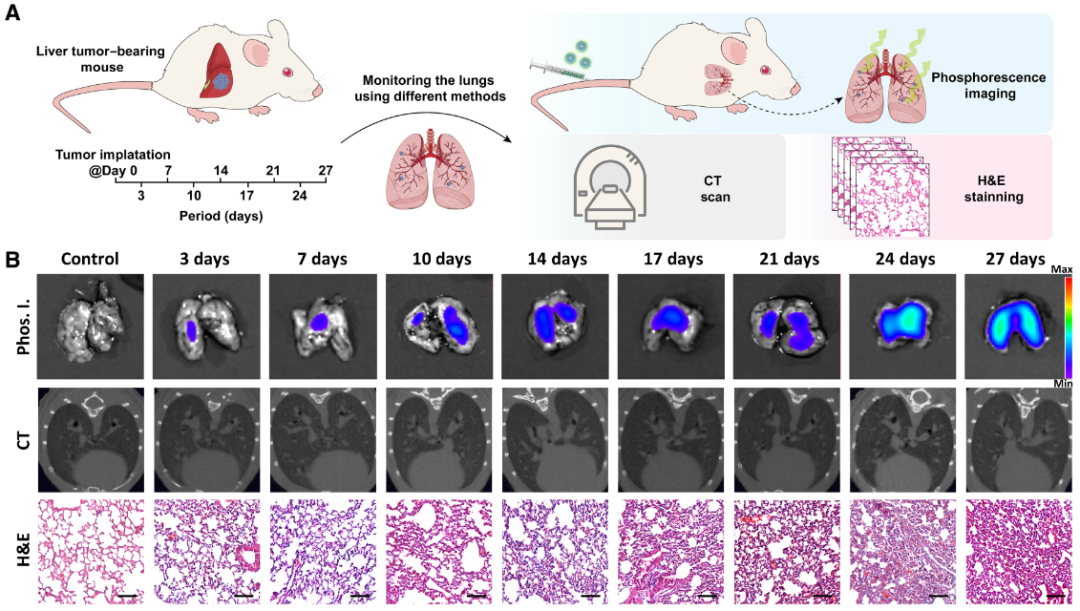
想要识别癌症早期转移,目前可用的体内成像方法并不少,但各有各的限制。例如,PET和CT对1cm以下的小肿瘤可靠性较低,MRI灵敏性不足,快速灵敏的荧光成像技术又必须考虑组织自发荧光带来的低信噪比,需要组织活检就更不用提了,难道把所有潜在的转移部位都依次取样吗?
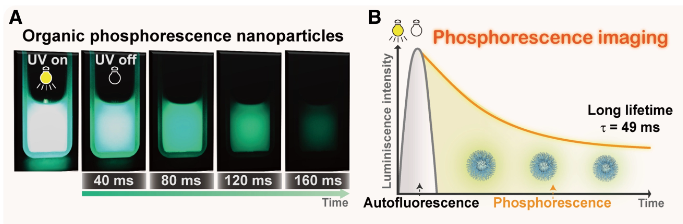
有机室温磷光材料(RTP)是一种新的成像剂,它有一些突出的优点。RTP能够在紫外光等激发源撤除之后还能保持一段时间的发光,因此能够避免组织自发荧光的影响,在低功率密度下,控制激发源开关即可获得高质量的光学影像。
研究者们制备了基于吩噻嗪衍生物的有机磷光纳米颗粒(NP),颗粒在水溶液中的磷光寿命可达49ms,比普通的RTP要长得多,发光肉眼可见。
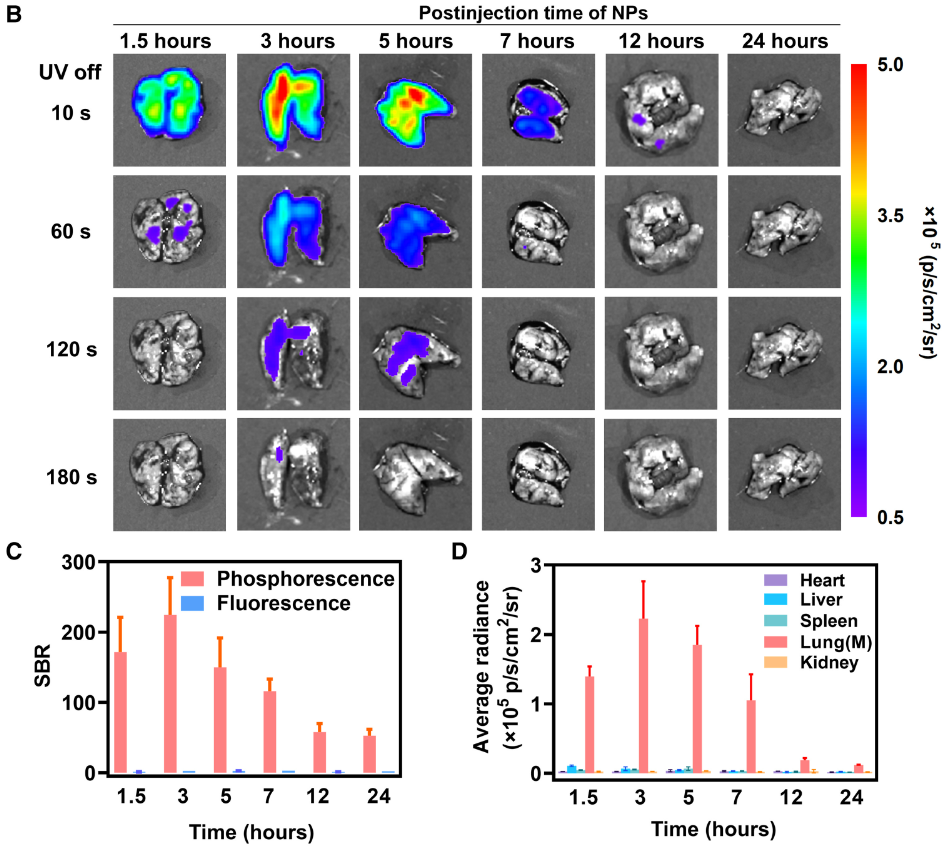
研究者将4T1癌细胞静脉注射到小鼠体内,建立肺转移模型,并在14天后给小鼠注射有机磷光纳米颗粒。成像结果显示,在心脏、肝脏、脾脏、肺和肾脏在内的主要器官中,只有肺出现了明显的磷光,可见有机磷光纳米颗粒对肺转移有较高的选择性。
由此可以说明,磷光标志的的确是肺转移的土壤。
参考资料:
[1]https://www.science.org/doi/10.1126/sciadv.adf6757
[2]https://news.whu.edu.cn/info/1015/69742.htm
文章来源:奇点网