用疫苗对抗癌症,尤其是成功治疗棘手的难治性癌症,可以说是无数人梦寐以求的事情。而今天发表在《自然》上的一项最新临床研究,就标志着治疗性癌症疫苗的研发,又往前迈进了一大步!
由基因泰克和BioNTech公司共同开发的mRNA个体化新抗原疫苗,在治疗胰腺癌的I期临床研究中,表现出良好的安全性和出色的疗效,50%的患者对疫苗治疗产生应答,且mRNA疫苗与化疗和免疫治疗的序贯联用,使胰腺癌的复发和患者死亡风险,较未实现应答的患者下降了92%(HR=0.08)[1]!
对抗5年生存率仅有12%,连免疫检查点抑制剂也束手无策的“癌中之王”,能取得如此优异的疗效,相信大家都和奇点糕一样好奇,mRNA个体化新抗原疫苗为什么这么秀呢?来一起看研究吧。
论文首页截图
科学界过去曾长期认为,免疫治疗对胰腺癌束手无策,一大关键原因就是胰腺癌的基因突变频率相对较低,可被T细胞识别的新抗原较少,再加上细胞外基质致密等因素,让胰腺癌成了缺少免疫细胞浸润的典型“免疫沙漠”。
不过,纪念斯隆-凯特琳癌症中心的研究团队分析了少数罹患胰腺癌后长期生存的幸存者,发现胰腺癌的新抗原含量其实并不低,但只有符合特定条件的少数“高质量新抗原”,才能充分激活T细胞;而在大多数情况下,新抗原并没能被有效呈递到T细胞,免疫系统没有目标,自然就袖手旁观了[2-3]。
为患者注射含有新抗原的个体化癌症疫苗,恰好就能“缺啥补啥”,解决“免疫系统缺少新抗原刺激”的问题,而肿瘤异质性所导致的不同患者个体间新抗原差异,也能通过“量身定制”疫苗来一并解决;mRNA疫苗技术的快速发展,特别是新冠疫情期间的突飞猛进,则让快速制备疫苗成为现实。
因此基因泰克、BioNTech两家公司的研究者们,与纪念斯隆-凯特琳癌症中心团队协力合作,组织了本次临床早期研究,以初步验证mRNA个体化新抗原疫苗autogene cevumeran的可行性和安全性,研究的具体流程如下:
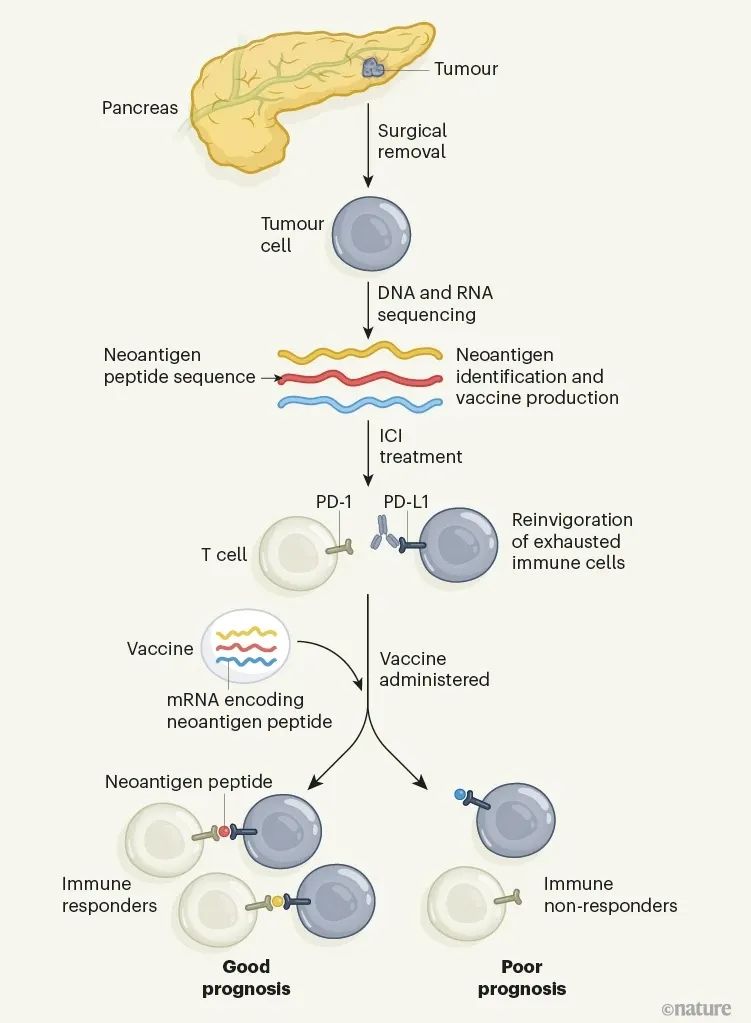
接受根治性手术切除的患者,术后先接受1剂PD-L1抑制剂阿替利珠单抗治疗,初步激活免疫应答,同时研究者们对肿瘤样本的DNA和RNA进行分析,筛选至多20个新抗原制备疫苗;此后,患者接受8剂autogene cevumeran注射,再行12个周期mFOLFIRINOX方案辅助化疗,最后注射1剂加强针疫苗。
研究整体流程图
研究共初步筛选了34例患者,但最终仅有16例患者成功接受autogene cevumeran治疗,15例按计划完成研究;疾病进展(7例)是导致患者退出研究的主要原因,也反映出胰腺癌的凶险,此外还有2例患者未能成功制备疫苗。
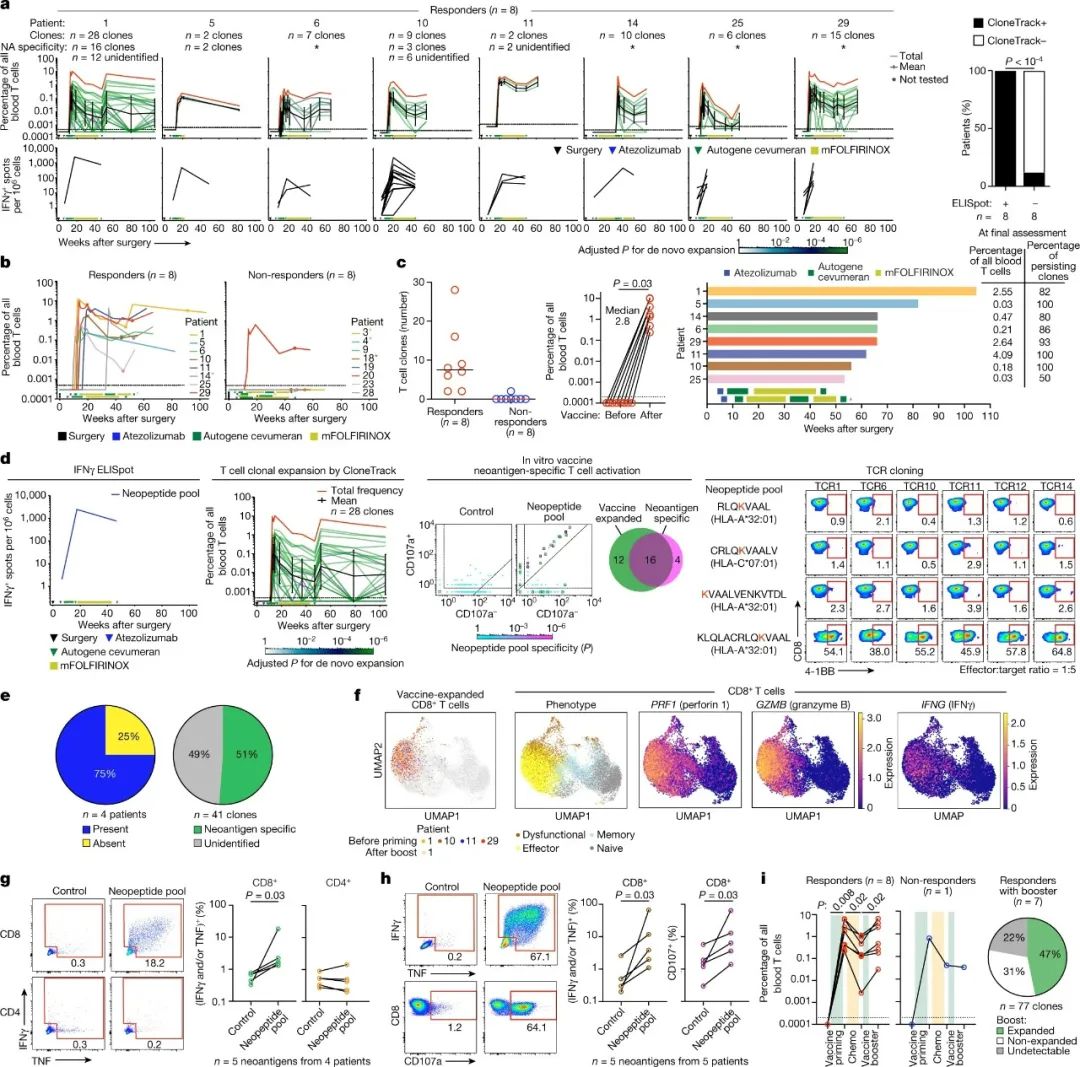
评价治疗是否有可行性,首先要看疫苗能不能真正激活T细胞:酶联免疫斑点分析(ELISpot)显示,8例患者在注射autogene cevumeran后,存在特异性针对疫苗所含新抗原(至少对1个新抗原有应答,实际中位个数为2)的CD8+T细胞免疫应答,而疫苗中约11%的新抗原是真正激活T细胞的高质量新抗原。
采用T细胞受体测序技术的进一步分析显示,被autogene cevumeran激活的CD8+T细胞,并不与阿替利珠单抗激活的T细胞重叠,但它们就足以高度特异性杀伤癌细胞,杀伤力也不受研究中辅助化疗的影响,也能较长久地存活。
不过研究者们也指出,对抗击肿瘤同样重要的CD4+T细胞并未被autogene cevumeran注射所激活,而另外8例患者未对疫苗产生应答,可能与肿瘤本身因素(肿瘤体积较大、突变多样性低)或手术切除患者脾脏(5例)有关,在小鼠身上开展的实验显示,切除脾脏会影响新抗原呈递和T细胞应答状态。
autogene cevumeran成功激活并扩增患者体内的CD8+T细胞
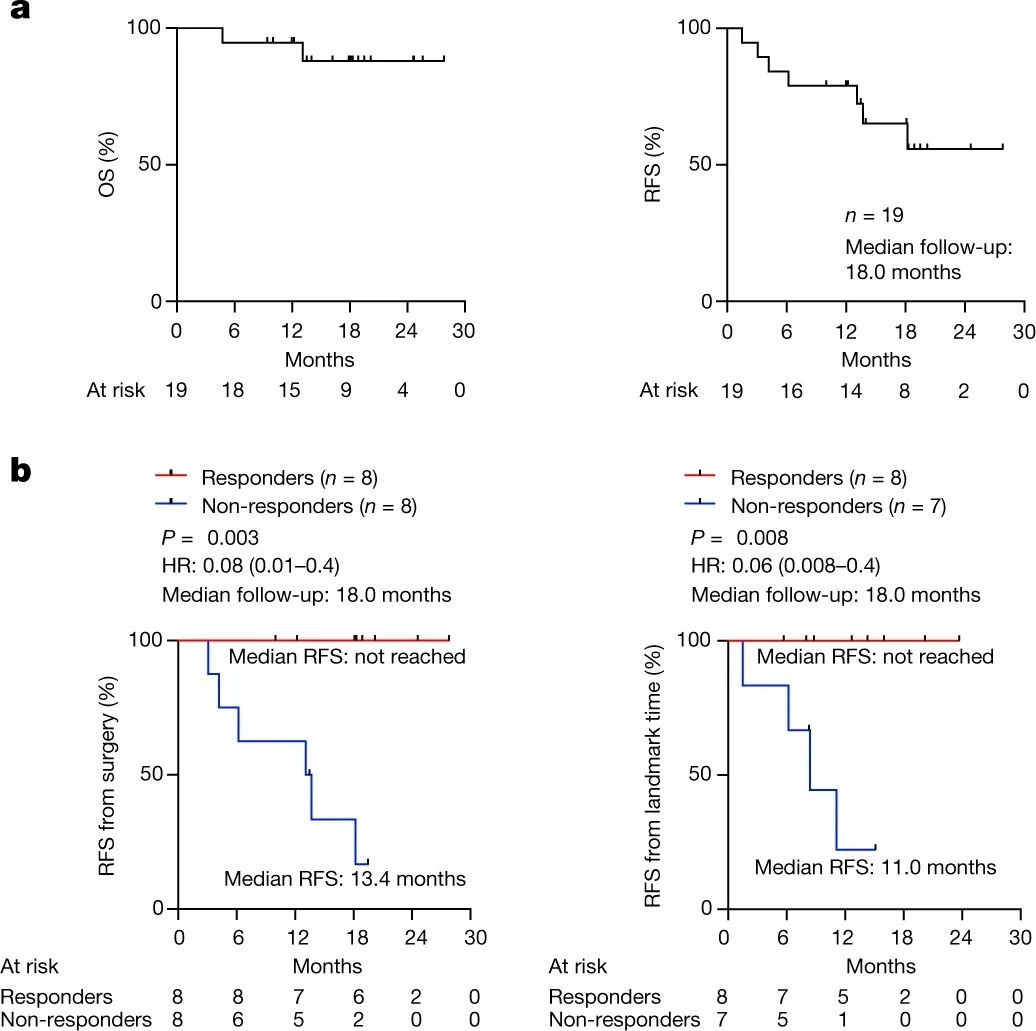
对autogene cevumeran疫苗产生应答,也显著改善了患者的临床结局:中位随访18个月时的数据显示,未应答的8例患者已有6例出现肿瘤复发或死亡,中位无复发生存期(RFS)为13.4个月,而有应答的8例患者仍全部安然存活,意味着autogene cevumeran使患者肿瘤复发或死亡的风险下降了92%!
生存曲线图
此外在安全性方面,autogene cevumeran疫苗也表现良好,仅有1例患者注射后出现3级不良事件(发热、高血压),但有3例患者因疾病进展、死亡或化疗毒性未能坚持注射完成全部疫苗;从患者手术结束到开始注射个体化疫苗,所需的中位时间为9.4周,速度也相当快了。
研究全程总结图
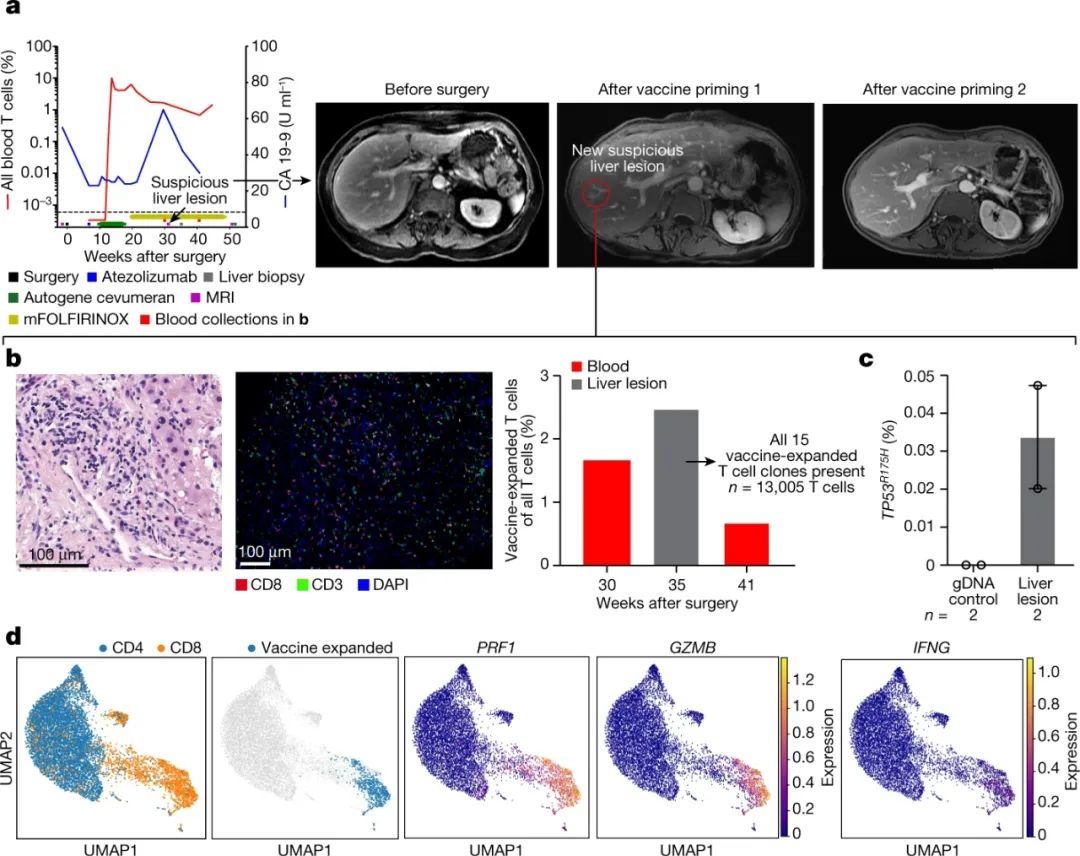
研究者们还分析了1例在接受辅助化疗期间疑似出现肝转移(大小为7mm,且病变处存在含有与原发灶相同TP53突变的罕见细胞)的患者,发现被autogene cevumeran疫苗激活和扩增的CD8+T细胞成功清除了此处病变,意味着个体化疫苗能助力胰腺癌患者清除微转移灶,这对改善患者的长期预后极为重要。
T细胞清除肝脏微转移灶
虽然作为一项样本量有限的临床I期研究,本次研究还不能充分证实mRNA个体化新抗原疫苗的疗效,但完全足以支持后续的全球性、多中心临床研究开展。研究者们还表示,近几年mRNA疫苗技术的飞跃式发展,意味着后续临床研究将使用制备更快、更为精准的疫苗,新疫苗的表现也许会更加惊艳!
参考文献:
[1]Rojas L A, Sethna Z, Soares K C, et al. Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer[J]. Nature, 2023.
[2]Balachandran V P, Łuksza M, Zhao J N, et al. Identification of unique neoantigen qualities in long-term survivors of pancreatic cancer[J]. Nature, 2017, 551(7681): 512-516.
[3]Łuksza M, Sethna Z M, Rojas L A, et al. Neoantigen quality predicts immunoediting in survivors of pancreatic cancer[J]. Nature, 2022, 606(7913): 389-395.
文章来源:奇点网