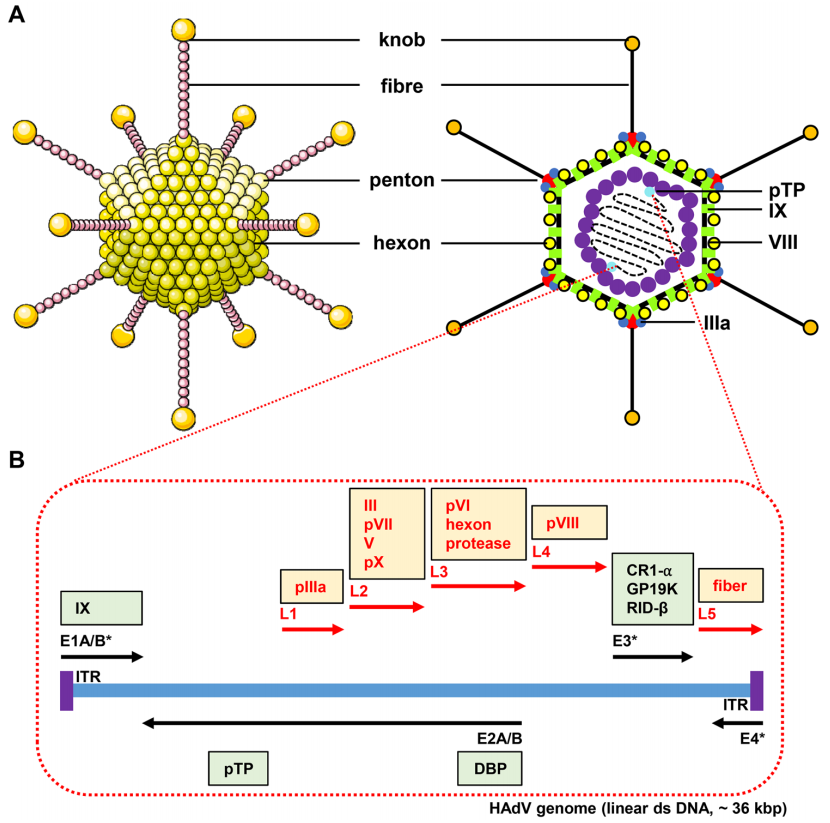
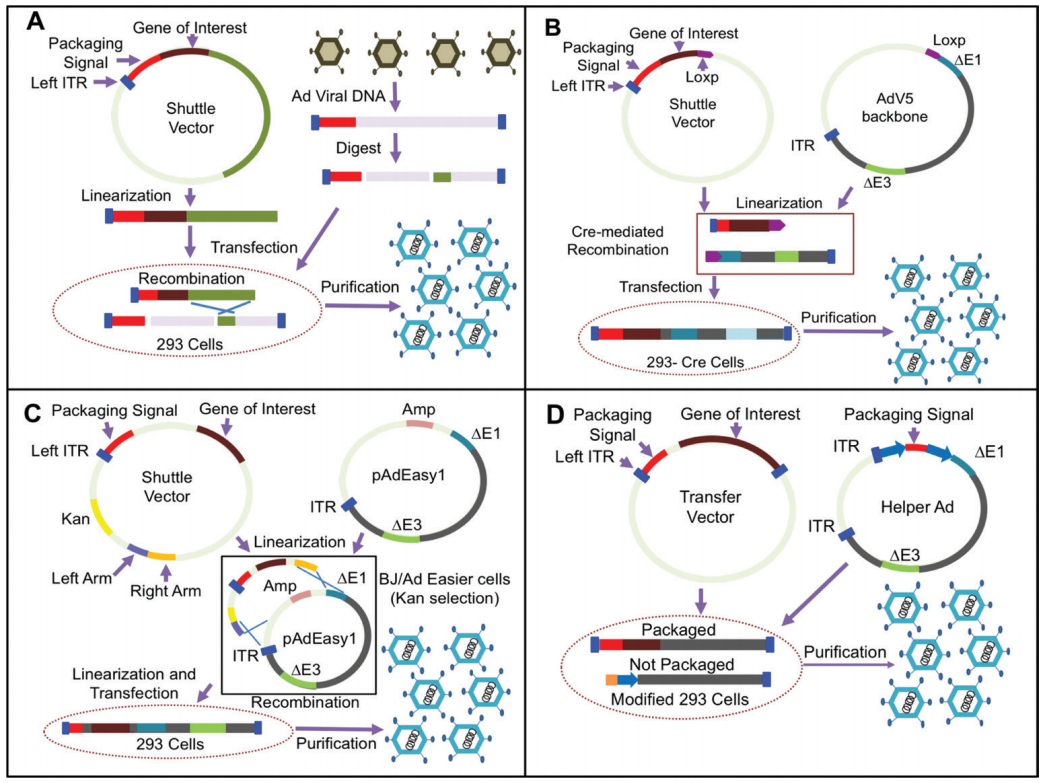
目前已知的腺病毒有52种,分别命名为Ad1~Ad52,其中Ad5是目前常用于改造成复制缺陷的腺病毒载体(Adenoviral Vector,AdV)的一种,其基因组是一个线性的36kb的dsDNA分子。Ad5缺失了腺病毒早期表达的基因序列E1和E3,其中,E1是腺病毒复制所必须的,因此,E1缺失使Ad不能完成自身复制,只能依靠包装细胞提供的反式互补方式进行复制扩增;E3编码的是细胞表面的一种糖蛋白,可对抗宿主的抗病毒防御系统,因此,E3的缺失可减少宿主免疫反应。近年来,腺病毒载体作为一种常用的基因操作工具,已被广泛用于基础研究、疫苗载体及基因治疗研究领域。
(2)共转染HEK293细胞;
(3)腺病毒收集:一般在转染后7~10d出现病变(CPE),80%的细胞出现CPE时,收集细胞上清和细胞,进行反复冻融,离心,收集上清后滤膜过滤,-80℃保存;
(4)腺病毒扩增:一般在感染后2~3d出现80~90%CPE,收集细胞,进行反复冻融,离心,收集上清后滤膜过滤,-80℃保存;
(5)腺病毒浓缩和纯化:PEG8000浓缩法;
(6)重组腺病毒鉴定:病毒滴度、质粒残留、宿主DNA残留、BSA残留、支原体检测、衣原体检测、内毒素检测、细菌及真菌检测等。
(1)宿主范围广:常用于感染难感染的细胞,不仅可感染普通细胞系,也可感染悬浮细胞、原代细胞等,以及感染增殖细胞、非增殖细胞;
(2)感染效率高:病毒滴度可高达1011PFU/mL,能有效进行增殖,适用于基因治疗;
(3)载体容量大:最高可容纳8kb外源DNA;
(4)表达快:感染细胞后,1~2天即可表达,是研究原代细胞及悬浮细胞基因表达的最佳选择;
(5)致病性低,安全性高:AdV携带的基因组不整合到宿主细胞的染色体中,不干扰其他宿主基因。
(2)若短期(7d内)使用病毒液,4℃保存即可;若需长期不用,请置于-80℃保存。反复冻融会降低病毒滴度(每次冻融会使病毒滴度降低10%~50%),因此在病毒使用过程中尽量避免反复冻融。
(2)若操作时生物安全柜内有病毒污染(病毒液体溅出),立即用70%乙醇加1%的SDS溶液擦拭干净。
(3)腺病毒包装相关实验使用过的枪头、细胞培养皿、EP管和废弃物等用消毒剂消毒、灭菌后(84消毒液和高温灭菌),再进行统一处理。
(4)腺病毒包装相关实验完毕后,仔细清洁双手。
Jt S, M H, Wam B, et al. Adenoviral vectors for cardiovascular gene therapy applications: a clinical and industry perspective.[J]. J Mol Med (Berl), 2022;100(6):875-901.
Singh S, Kumar R, Agrawal B. Adenoviral Vector-Based Vaccines and Gene Therapies: Current Status and Future Prospects[M]. 2018.