胰腺癌(PaCa)是最常见的恶性肿瘤之一,不幸的是,由于缺乏有效的治疗和诊断方法,导致预后不良,死亡率极高。迄今为止,PaCa发病机制和进展机制尚不清楚。
外泌体是由大多数细胞分泌的小囊泡,含有脂质、蛋白质和核酸等,并参与多种细胞功能,如细胞间通讯、生物过程和细胞信号传导等。在PaCa中,外泌体富含多种信号分子,可调控免疫抑制介导细胞间通讯,影响胰腺星状细胞和胰腺癌细胞之间的相互促进,以及正常细胞的重编程;其还可调节PaCa微环境,促进PaCa生长和存活;也可建立转移前的微生态位,促进PaCa靶向。总之,外泌体作为PaCa靶向药物的生物标志物介质具有重要的临床价值。
2022年1月15日,扬州大学临床医学院苏北人民医院普外科研究所Huan Zhang团队在Cell Communication and Signaling上发表了题为“Exosomes: the key of sophisticated cell–cell communication and targeted metastasis in pancreatic cancer”的综述性论文。在本文中,团队就PaCa来源的外泌体转运信号功能、介导细胞间通讯以及调控PaCa转移等方面进行综述。
外泌体的产生始于胞吞作用,然后是复杂的胞内途径,最后才是胞浆胞吐作用(图1A)。有研究表明,与正常细胞相比,癌细胞分泌更多的外泌体。包裹外泌体的脂质双分子层中含有多种信号分子,如抗原呈递分子、整合素、表面蛋白聚糖、CD9、CD63、CD81等,可介导外泌体的识别和融合、摄取和分泌(图1B)。外泌体携带的大量细胞信号分子,可调节细胞间通讯以及附近的PaCa微环境,随后促进PaCa侵袭和转移。
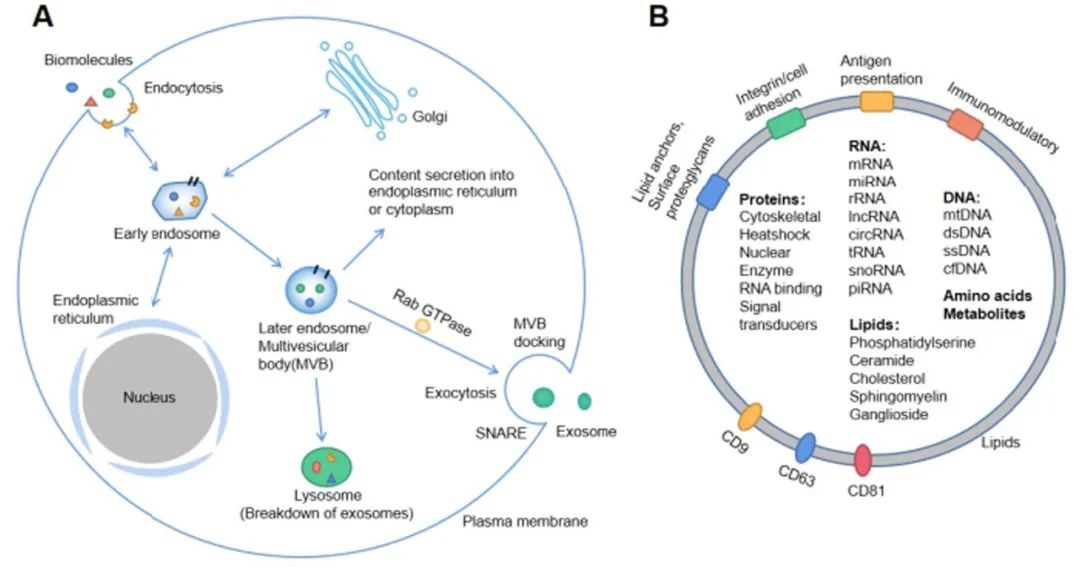
图1 A 起源:液体和细胞外成分与细胞表面蛋白一起通过内吞作用和质膜融合进入细胞,形成早期内涵体;随后,早期内体可通过与细胞内物质(如高尔基体和细胞质中的内质网)进行信息交换,介导各种机制形成晚期内涵体(MVBs);最后,MVBs与细胞质交换信息,通过溶酶体降解或通过Rab GTPase和SNARE蛋白介导,到达细胞膜释放外泌体。B 结构:外泌体表面蛋白包括整合素、免疫调节蛋白等;外泌体含有不同的细胞表面蛋白、细胞内蛋白、RNA、DNA、氨基酸和代谢物。
目前,广泛接受的细胞间通信模式包括(1)化学感受器介导的接触;(2)细胞间的直接接触;(3)细胞-细胞突触接触。一方面,PaCa分泌的Pex可将供体细胞的核酸、蛋白质和脂质转运至受体细胞,释放诱导炎症反应、抑制免疫反应、调节癌细胞抗凋亡反应和促血管生成的信号,从而促进癌症转移。另一方面,与PaCa相关的细胞,如肿瘤相关巨噬细胞(TAMs)、肿瘤起始细胞(CICs)和胰腺星状细胞(PSCs)释放的外泌体,可促进PaCa生长、耐药、转移和侵袭(图2)。
 外泌体是PaCa器官特异性转移的关键决定因素,这是通过不同整合素(ITG)表达水平实现的。ITG可通过激活Src磷酸化和促炎细胞S100的表达,与器官特异性驻留细胞融合,建立转移前生态位,从而确定转移灶是否为嗜器官性转移。最容易被PaCa转移的器官是肝脏和肺。在PaCa肝转移中,表达ITGαvβ5的外泌体可特异性结合到肝kupffer细胞,Pex通过体液途径与kupffer细胞融合运输到肝脏(图3)。
外泌体是PaCa器官特异性转移的关键决定因素,这是通过不同整合素(ITG)表达水平实现的。ITG可通过激活Src磷酸化和促炎细胞S100的表达,与器官特异性驻留细胞融合,建立转移前生态位,从而确定转移灶是否为嗜器官性转移。最容易被PaCa转移的器官是肝脏和肺。在PaCa肝转移中,表达ITGαvβ5的外泌体可特异性结合到肝kupffer细胞,Pex通过体液途径与kupffer细胞融合运输到肝脏(图3)。
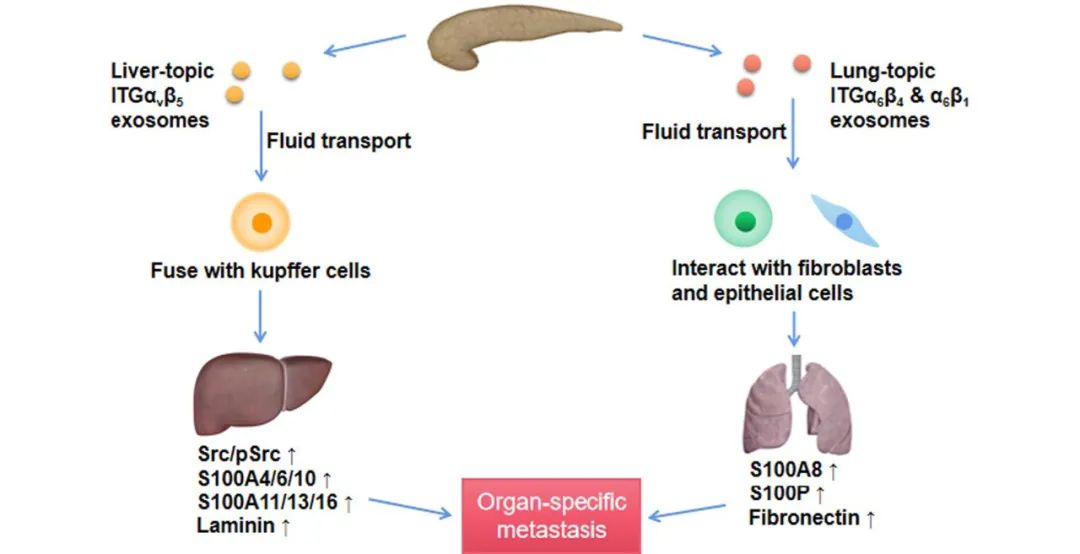 图3 Pex通过整合素直接导致器官特异性转移示意图。
Cell Commun Signal. 2022 Jan 15.
doi: 10.1186/s12964-021-00808-w.
Exosomes: the key of sophisticated cell-cell communication and targeted metastasis in pancreatic cancer
Pancreatic cancer is one of the most common malignancies. Unfortunately, the lack of effective methods of treat-ment and diagnosis has led to poor prognosis coupled with a very high mortality rate. So far, the pathogenesis and progression mechanisms of pancreatic cancer have been poorly characterized. Exosomes are small vesicles secreted by most cells, contain lipids, proteins, and nucleic acids, and are involved in diverse functions such as intercellular communications, biological processes, and cell signaling. In pancreatic cancer, exosomes are enriched with multiple signaling molecules that mediate intercellular communication with control of immune suppression, mutual promo-tion between pancreas stellate cells and pancreatic cancer cells, and reprogramming of normal cells. In addition, exosomes can regulate the pancreatic cancer microenvironment and promote the growth and survival of pancreatic cancer. Exosomes can also build pre-metastatic micro-ecological niches and facilitate the targeting of pancreatic can-cer. The ability of exosomes to load cargo and target allows them to be of great clinical value as a biomarker mediator for targeted drugs in pancreatic cancer.
关键词:Pancreatic cancer (PaCa), Exosome, Cell–cell communication, Metastasis, Biomak
图3 Pex通过整合素直接导致器官特异性转移示意图。
Cell Commun Signal. 2022 Jan 15.
doi: 10.1186/s12964-021-00808-w.
Exosomes: the key of sophisticated cell-cell communication and targeted metastasis in pancreatic cancer
Pancreatic cancer is one of the most common malignancies. Unfortunately, the lack of effective methods of treat-ment and diagnosis has led to poor prognosis coupled with a very high mortality rate. So far, the pathogenesis and progression mechanisms of pancreatic cancer have been poorly characterized. Exosomes are small vesicles secreted by most cells, contain lipids, proteins, and nucleic acids, and are involved in diverse functions such as intercellular communications, biological processes, and cell signaling. In pancreatic cancer, exosomes are enriched with multiple signaling molecules that mediate intercellular communication with control of immune suppression, mutual promo-tion between pancreas stellate cells and pancreatic cancer cells, and reprogramming of normal cells. In addition, exosomes can regulate the pancreatic cancer microenvironment and promote the growth and survival of pancreatic cancer. Exosomes can also build pre-metastatic micro-ecological niches and facilitate the targeting of pancreatic can-cer. The ability of exosomes to load cargo and target allows them to be of great clinical value as a biomarker mediator for targeted drugs in pancreatic cancer.
关键词:Pancreatic cancer (PaCa), Exosome, Cell–cell communication, Metastasis, Biomak




