自古以来就有皇帝、圣人炼丹制药以寻求长生不老之道的历史传统。而随着经济水平的发展,平均预期寿命不断提高,人口老龄化及衰老的问题越来越突出,因此不论是科学家还是普罗大众,都希望寻找一方良药来减缓衰老甚至延长寿命。
近期,来自葡萄牙波尔图大学的Elsa Logarinho团队找到了一方良药——转录因子FOXM1,并通过小鼠体内实验证实它具有减缓衰老,延长寿命的作用。在自然衰老小鼠中,提高FOXM1表达可显著延长中位寿命28%和最大寿命29%,也减缓了衰老相关的体重下降!
这项研究成果近期发表在顶级衰老研究期刊Nature Aging上[1],让我们一起来康康吧!
论文首页截图
在该课题组既往研究中,他们在HGPS(Hutchinson–Gilford progeria syndrome,早老症)患者来源的成纤维细胞中过表达FOXM1的N端截短型形式(简称FOXM1-dNdK),增强了细胞的增殖能力,同时延缓了细胞过早衰老的发生。这一部分体外的结果已于2018年在Nature Communications上发表[2]。
注:HGPS,早老症,一种早发而严重的过早老化性疾病,它是由于编码A/C型核纤层蛋白的LMNA基因发生点突变而引起。因为HGPS由已知基因突变引起,研究者很容易构建相应的小鼠模型。且因为正常衰老进程是一个很缓慢的过程(即使在小鼠,通常也需要2-3年),而HGPS大大加速了衰老的进程,因此在衰老研究中常选择HGPS小鼠或人的细胞样本作为衰老研究模型。
既然体外有疗效,那体内效果如何?为了回答这个问题,研究者采用了自然衰老小鼠和HGPS小鼠[3](LmnaG609G/G609G,简称LAKI)来进行研究,在这两种小鼠中过表达FOXM1来分别观察在生理性衰老和病理性衰老中是否可以产生抗衰疗效。
首先,研究者构建了一个转基因小鼠,简称为LAKI-Foxm1,这个小鼠具备HGPS表型,同时可以通过多西环素(dox)诱导的方式过表达截短的FOXM1。研究者利用该小鼠的耳真皮成纤维细胞,在体外测试了短期过表达FOXM1-dNdK的效率和细胞衰老表型的变化。(这一部分实验和他们在Nature Communications中的实验一样,只不过这里把HGPS患者的成纤维细胞换成了LAKI-Foxm1小鼠的成纤维细胞。)
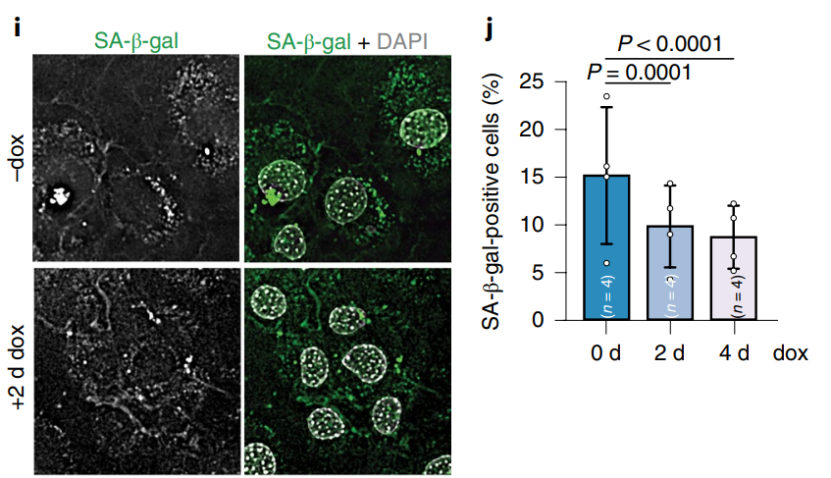
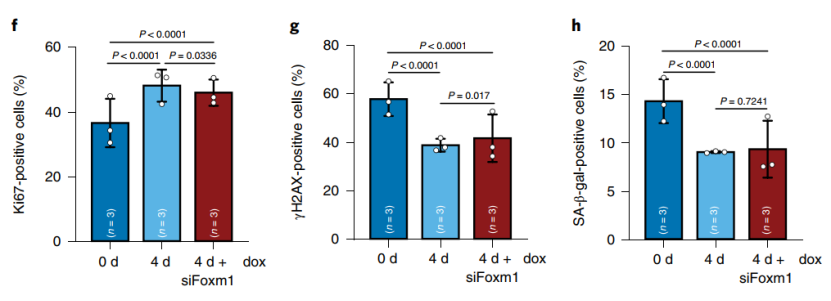
结果显示该系统可将FOXM1过表达5-10倍,包括细胞增殖(Ki67)、DNA损伤(γH2AX)、细胞衰老经典marker(SA-β-gal)、异染色质相关的表观marker(H3K9me3/H4K20me3)、核膜完整性和核面积等指标均显示过表达FOXM1可以减轻细胞衰老表型。
在小鼠成纤维细胞中过表达FOXM1可以减轻细胞衰老表型
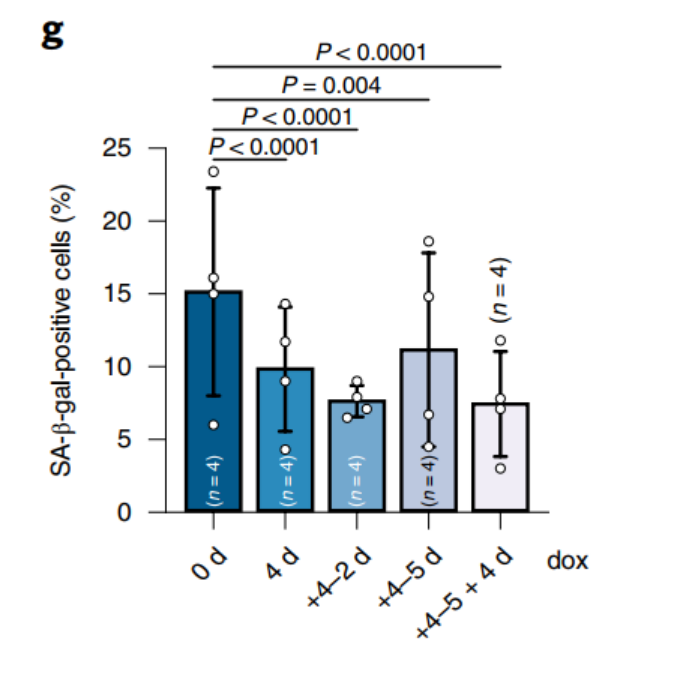
结果显示即使撤除FOXM1过表达5天后,虽然衰老表型有一定的积累,但仍能够较好的维持先前4天过表达FOXM1对细胞衰老表型的改善,与未处理的成纤维细胞差异显著。更让人振奋的是,在撤除dox 5天后再次给予dox过表达FOXM1能够进一步阻止衰老表型的再积累。
过表达FOXM1的抗衰获益具有维持效应
研究者想先看看这个潜在治疗方式是否对病理性衰老有预防作用,而不是逆转作用(早期干预相较晚期逆转可能更易获得治疗阳性结果),因此研究者选用了从4周龄小鼠开始持续上述给dox的策略12周至小鼠16周龄来观察。
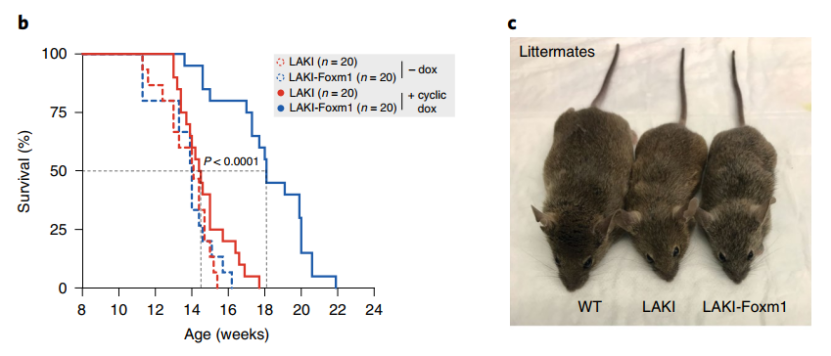
结果显示,与LAKI对照组相比,dox饮食下的LAKI-Foxm1小鼠的中位寿命和最大寿命延长了约25%(中位,18.1周 vs 14.4周;最大,21.9周 vs 17.7周),且HGPS小鼠中出现的体重下降和生长发育迟缓也在治疗后得以改善。值得注意的是,dox处理的LAKI-Foxm1小鼠的尸检分析并未显示任何增生组织生长的明显迹象,说明具有一定安全性(至少没有长出肉眼可见的瘤子)。
LAKI(HGPS)小鼠中过表达FOXM1能够延长小鼠寿命
病理性衰老小鼠中过表达FOXM1后驼背症状得到改善
接下来,研究者在组织层面(包括皮肤、脂肪、主动脉、骨骼)和分子水平进一步验证了FOXM1对病理性衰老表型的治疗改善效果。各组织在病理层面的衰老变化均有所改善。
重要的是,LAKI小鼠皮肤、性腺脂肪和主动脉中上调的几种衰老marker在LAKI-foxm1小鼠中均恢复到WT水平。
以上是在病理性衰老,也就是HGPS模型小鼠中得到的结果,然而病理性衰老并不能完全代表生理性衰老,从其发病机制可以看出病理性衰老主要是某一基因突变导致的,而自然衰老是全局性的广泛改变,二者存在本质区别。
因此,研究者想进一步探究FOXM1过表达是否可以改善自然衰老小鼠的衰老表型?
FOXM1作为一个重要的细胞周期转录因子,过表达确实会促进细胞增殖分裂,而长时间“循环”过表达时就不得不考虑其致癌性。且研究报道,癌症中高FOXM1水平与不良临床结局之间存在关联,因此,研究者对该方法的致瘤风险提出了质疑。首先得排除较大的风险,才能谈治疗效果~
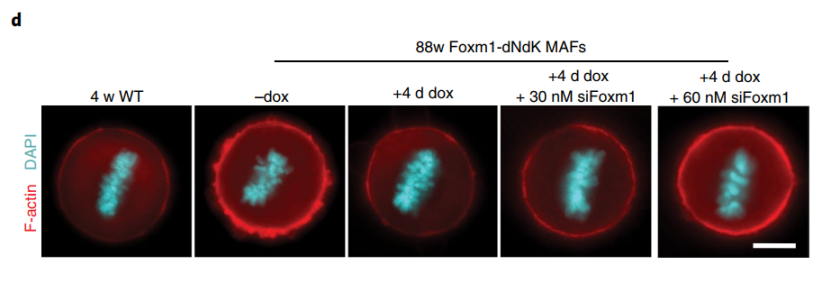
碰巧的是,近期有证据揭示了FOXM1的非转录端(N端)具有肿瘤抑制功能[4]。且研究者用88周龄Foxm1-dNdk老年小鼠的成纤维细胞(MAF)与4周龄MAF进行体外实验证实了FOXM1-dNdK诱导确实可逆转致瘤表型,但具体而言是通过上调内源性Foxm1来起到作用,siRNA干扰内源性Foxm1后致瘤表型恢复证实了这一点。
自然衰老小鼠成纤维细胞中证实FOXM1过表达具有抑瘤效果
(F-actin:皮层肌动蛋白,与肿瘤发生和转移灶形成正相关)
自然衰老小鼠成纤维细胞的衰老表型被转基因FOXM1的转录功能所改善
既然目前的证据显示该治疗方法在致瘤性方面是安全的,那接下来就要看看在自然衰老小鼠中的抗衰效果了。
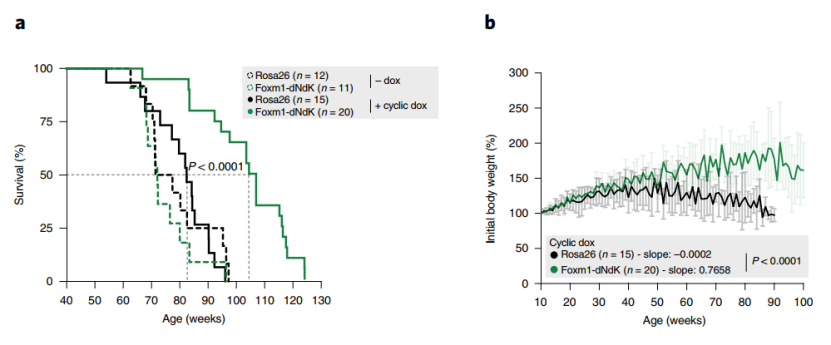
研究者采用8周龄Foxm1-dNdK小鼠,按“给3天dox,停4天dox”的策略过表达FOXM1,共80周,至88周时检测衰老组织表型(皮肤、肌肉、脂肪、主动脉)和分子水平的变化(RNA-seq)。整个过程中持续记录生存曲线和体重变化。
过表达FOXM1减缓衰老进程、延长自然衰老小鼠寿命
对组织表型的检测结果显示,治疗组相较对照组背侧皮肤组织稳态改善,皮下脂肪显著增加;性腺脂肪沉积中脂肪细胞大小有轻微的改善;年龄相关的肌纤维萎缩轻度逆转;主动脉衰老表型即外膜纤维化、主动脉壁增厚和血管平滑肌细胞丢失均有显著逆转。
值得注意的是,为了证明衰老表型确实减弱,而不仅仅是由于FOXM1过表达产生的广谱益处(gain-of-function),研究者在一个不存在衰老相关表型的阶段(14-16周龄),评估了FOXM1转基因过表达对幼年动物组织的影响。结果显示以上在组织层面检测的表型指标没有显著变化。提示这不是一个单纯的gain-of-function,而确实是针对衰老表型的治疗作用。
接下来研究者做了两组小鼠主动脉和腓肠肌组织的bulk RNA-seq,观察分子层面的变化以及试图解析潜在的抗衰老分子机制。GSEA分析显示在两种组织中均发生改变的通路主要为炎症和代谢通路。分子水平变化特征上,该疗法与其他已知抗衰老疗法类似。
N末端截短的FOXM1循环表达可改善健康和寿命
需要注意的是,上述病理性衰老和生理性衰老的小鼠实验用到的干预措施均是预防性长期干预,而不是在衰老中晚期进行真正意义上的治疗。
在细胞和小鼠中预防性治疗效果如此好,期待研究者进一步推进衰老中晚期治疗及相关大动物实验并阐明具体的分子机制,希望够成为早衰症和自然衰老的治疗靶点添砖加瓦。
参考资料:
1. Ribeiro, R., et al., In vivo cyclic induction of the FOXM1 transcription factor delays natural and progeroid aging phenotypes and extends healthspan. Nature Aging, 2022. 2(5): p. 397-411.
2. Macedo, J.C., et al., FoxM1 repression during human aging leads to mitotic decline and aneuploidy-driven full senescence. Nat Commun, 2018. 9(1): p. 2834.
3. Osorio, F.G., et al., Splicing-directed therapy in a new mouse model of human accelerated aging. Sci Transl Med, 2011. 3(106): p. 106ra107.
4. Limzerwala, J.F., et al., FoxM1 insufficiency hyperactivates Ect2-RhoA-mDia1 signaling to drive cancer. Nat Cancer, 2020. 1(10): p. 1010-1024.
文章来源:奇点网